
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源:不详 题型:填空题
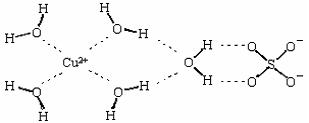
| A.水 | B.四氯化碳 | C.苯 | D.硫酸镍溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
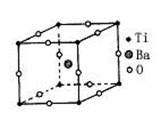
| A.BaTi8O12 | B.BaTi4O6 |
| C.BaTi2O4 | D.BaTiO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
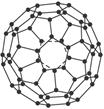
| A.C18 | B.C44 | C.C72 | D.C83 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 极为丰富的元素。
极为丰富的元素。 N的键能为942 kJ·mol-1,N-N单键的键能为247 kJ·mol-1,计算说明N2中的___________键比____________键稳定(填“σ”或“π”)。
N的键能为942 kJ·mol-1,N-N单键的键能为247 kJ·mol-1,计算说明N2中的___________键比____________键稳定(填“σ”或“π”)。 (白圆圈代表N3-离子)
(白圆圈代表N3-离子)
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碘和氯化钾 | B.金刚石和重晶石 |
| C.二氧化硅和干冰 | D.软脂酸甘油酯和冰醋酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NH4NO3、NaOH中既有离子键,又有极性共价键,其中NH4NO3中还有配位键 |
| B.水的沸点是100℃,硫化氢的分子结构跟水相似,但它的沸点却很低,是-60.7℃,引起这种差异的主要原因是水分子间有氢键 |
| C.范德华力与氢键可同时存在于分子之间 |
| D.氢键比范德华力强,且氢键是一种特殊的化学键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子化合物中可能含有非极性键 | B.分子晶体中不含离子键 |
| C.原子晶体中可能含有非极性键 | D.分子晶体中一定有共价键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com