
 mol,
mol, ,
, ;
;

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解

| V3-(V2-V1) |
| 22400m |
| V3-(V2-V1) |
| 22400m |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:

图6 图7
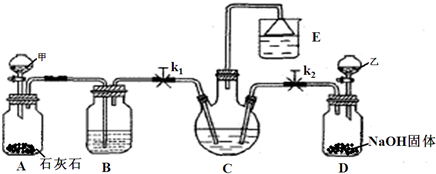
(1)上述生产纯碱的方法称________________,副产品的一种用途为____________________。
(2)沉淀池中发生的化学反应方程式是________________________________________。
(3)写出上述流程中X物质的分子式________________________________。
(4)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了_________(填上述流程中的编号)的循环。从沉淀池中取出沉淀的操作是_____________________________。
(5)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加________________。
(6)向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有______________。
a.增大![]() 的浓度,使NH4Cl更多地析出
的浓度,使NH4Cl更多地析出
b.使NaHCO3更多地析出
c.使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com