
| A、c(H+):c(OH-)=1:2的溶液:K+、Al3+、HCO3-、ClO- |
| B、与Al反应生成H2的溶液:Na+、Ba2+、NO3-、Cl- |
| C、中性溶液中:SO32-、S2-、Fe3+、Cl- |
| D、能使红色酚酞变无色的溶液:K+、Ca2+、Cl-、HCO3- |


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案科目:高中化学 来源: 题型:
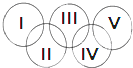 如右图,假定五环中的一环表示一种物质,相连环物质间一定条件下能发生常见反应,不相连环物质间不能发生反应,且四种反应中必须包含化合反应、置换反应及复分解反应,适合的一组是( )
如右图,假定五环中的一环表示一种物质,相连环物质间一定条件下能发生常见反应,不相连环物质间不能发生反应,且四种反应中必须包含化合反应、置换反应及复分解反应,适合的一组是( )| Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | |
| A | SiO2 | NaOH溶液 | CuSO4溶液 | Ag | O2 |
| B | O2 | Fe | 稀H2SO4 | NaOH溶液 | CO2 |
| C | O2 | NH3 | 稀H2SO4 | NaOH溶液 | Al |
| D | Mg | Al | CO2 | Fe2O3 | KOH溶液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、仅①③④⑤ | B、仅②③④ |
| C、仅①③④ | D、仅①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
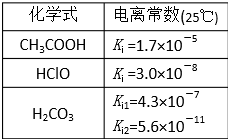
| A、c(H+)=1×10-14mol/L的溶液:K+、Na+、AlO2-、S2O32- |
| B、上表提供的数据下:HClO、HCO3-、ClO-、CO32- |
| C、能与Al反应生成H2的溶液:NH4+、Ca2+、NO3-、I- |
| D、中性的溶液中:CO32-、Na+、SO42-、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-.向含3mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示.
已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-.向含3mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解质的电离是在通电的条件下进行的 |
| B、强电解质溶液的导电能力不一定比弱电解质溶液强 |
| C、盐酸是强电解质,所以盐酸中没有HCl分子 |
| D、H2O(g)═H2O(l)是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、发生有效碰撞的分子一定是活化分子 |
| B、活化分子间的碰撞一定是有效碰撞 |
| C、能发生有效碰撞的分子必须具有相当高的能量 |
| D、使用催化剂能改变分子的活化能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 有一瓶澄清溶液,其中可能含有NH4+、K+、Ba2+、Al3+、Fe3+、Mg2+、I-、NO3-、CO32-、SO42-、AlO2-.取该溶液进行以下实验:
有一瓶澄清溶液,其中可能含有NH4+、K+、Ba2+、Al3+、Fe3+、Mg2+、I-、NO3-、CO32-、SO42-、AlO2-.取该溶液进行以下实验:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com