
| A. | 稀硫酸滴在银片上:2Ag+2H+═2Ag++H2↑ | |
| B. | 碳酸钠与稀盐酸的反应:CO32-+2H+═H2O+CO2↑ | |
| C. | Mg(OH)2与盐酸的反应:H++OH-═H2O | |
| D. | 铜片放入ZnSO4溶液中:Cu+Zn2+═Cu2++Zn |
分析 A.银的活泼性较弱,不与稀硫酸反应;
B.碳酸钠与稀盐酸反应生成氯化钠、二氧化碳气体和水;
C.氢氧化镁为难溶物,离子方程式中氢氧化镁不能拆开;
D.铜的活泼性小于Zn,铜不与硫酸锌反应.
解答 解:A.金属Ag的活泼性较弱,不会与稀硫酸反应,该反应不会发生,故A错误;
B.碳酸钠与稀盐酸的反应生成氯化钠、二氧化碳和水,反应的离子方程式为:CO32-+2H+═H2O+CO2↑,故B正确;
C.Mg(OH)2与盐酸的反应生成氯化镁和水,氢氧化镁不能拆开,正确的离子方程式为:2H++Mg(OH)2═Mg2++2H2O,故C错误;
D.铜的活泼性小于Zn,反应Cu+Zn2+═Cu2++Zn不会发生,故D错误;
故选B.
点评 本题考查了离子方程式的判断,题目难度不大,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 在多电子的原子里,能量高的电子通常在离核近的区域内活动 | |
| B. | 核外电子总是先排在能量低的电子层上,例如只有排满了L层后才排M层 | |
| C. | 两种微粒,若核外电子排布完全相同,则其化学性质一定相同 | |
| D. | 微粒的最外层只能是8个电子才稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
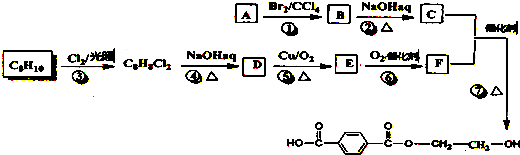
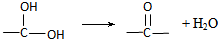
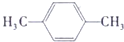 .
.

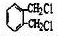 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在周期表中,元素的族序数都等于其原子的最外层电子数 | |
| B. | 周期表中非金属性最强的元素,其最高价氧化物的水化物酸性也最强 | |
| C. | 同主族元素随原子核电荷数的递增,原子半径依次减小 | |
| D. | ⅦA族元素的单质,随分子量的增大,熔、沸点升高;ⅠA族单质,随分子量的增大,熔、沸点降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 化合物 | 甲 | 乙 | 丙 | 丁 |
| 组成元素 | B、C | A、C | A、D | C、D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/浓度 | c(NH3)(mol/L) | c(O2 )(mol/L) | c(NO)(mol/L) |
| 起始 | 0.800 | 1.000 | 0.000 |
| 第2min | a | b | c |
| 第4min | 0.400 | 0.500 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com