
【题目】不法分子有时用铜锌合金制成假金币行骗。下列方法中,不能有效鉴别真假的是
A. 在空气中灼烧看表面是否变黑
B. 利用阿基米德原理测密度
C. 用手掂量轻重
D. 滴一滴硝酸在金币的表面,观察现象
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】以淀粉为主要原料合成一种具有果香味的物质C和化合物D的合成路线如下图所示。
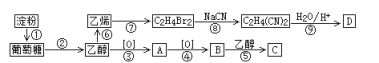
已知:R-CN![]() R-COOH
R-COOH
请回答下列问题:
(1)D的结构简式为____________________;
(2)反应⑧的类型为___________,B分子中的官能团名称为___________;
(3)反应⑤的化学方程式为_______________________;
(4)A发生银镜反应的化学方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学选修-物质结构与性质】
已知前四周期六种元素A、B、C、D、E、F的原子序数之和为107,且它们的核电荷数依次增大,B原子的p轨道半充满,其氢化物沸点是同族元素中最低的,D原子得到一个电子后3p轨道全充满,A与C能形成A2C型离子化和物,其中的阴、阳离子相差一个电子层,E4+离子和氩原子的核外电子排布相同.请回答下列问题:
(1)A、B、C、D的第一电离能由小到大的顺序是______(填元素符号)
(2)化合物BD3的分子空间构型可描述为______,B的原子轨道杂化类型为______。
(3)已知F元素在人体内含量偏低时,会影响O2在体内的正常运输.已知F2+与KCN溶液反应得F(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物.则F的基态原子价电子排布式为______。CN-与______(一种分子)互为等电子体,则1个CN-中π键数目为______。
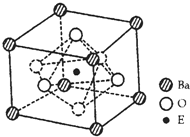
(4)EO2与碳酸钡在熔融状态下反应,所得晶体的晶胞结构如图所示,则该反应的化学方程式为______,
在该晶体中,E4+的氧配为数为______。若该晶胞边长为anm可计算该晶体的密度为______g/cm3(阿伏加德罗常数为NA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量的O2和NH3混合成448 mL,通过预先加热的催化剂三氧化二铬充分反应后,再通过足量的水,最终收集到44.8mL的无色气体。则原混合气体中O2的体积可能是(氨全部被氧化;气体体积均已换算成标准状况)( )
A. 231.5 mLB. 268.8 mLC. 287.5 mLD. 56 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G均为芳香族化合物,有如下转化关系:![]()
(1)有机物C的分子式为C8H10O2 , 核磁共振氢谱显示3组峰,C不能与NaOH反应,写出C的结构简式___ . 上述反应中属于取代反应的是___(填数字序号).
(2)写出反应②、③的化学方程式:___;___ .
(3)1mol D与足量的银氨溶液完全反应生成E,E是合成纤维涤纶的一种单体,另一种单体是C,写出合成涤纶的化学方程式___ .
(4)1mol E、F(F的式量小于E)完全燃烧,消耗O2的量相等,且1 mol F能和1mol NaOH完全反应,写出F的结构简式___ .
(5)G的分子式为C8H8O4 , 且知苯环上的一氯取代物只有两种,G不与NaHCO3反应,能与Na和NaOH反应,等质量的G消耗Na和NaOH的物质的量之比为2:3,则符合上述条件G的结构简式为___(写出一种).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是一种重要的化工原料,以乙烯为原料衍生出部分化工产品的反应如下(部分反应条件已略去)。
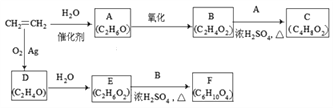
请回答下列问题:
(1)A物质的名称是_________________________。
(2)B和A反应生成C的化学方程式为__________________________________,该反应的类型为____________________。
(3)D为环状化合物,其同分异构体与银氨溶液反应的化学方程式为____________。
(4)F的结构简式为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA。下列说法正确的是( )
A. 1 L 0.1 mol·L-1 NH4Cl溶液中,NH4+的数量为0.1NA
B. 1mol Na2O2与足量的水反应,转移的电子数为2NA
C. 标准状况下,2.24 L N2和O2的混合气体中分子数为0.2NA
D. 0.1 mol H2和0.1 mol I2于密闭容器中充分反应后,其分子总数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项中表达正确的是( )
A. 第VⅡA族元素形成的氢化物中沸点最高的是HI
B. 水分子很稳定性是因为水分子间易形成氢键
C. 用电子式表示HCl形成过程:![]()
D. 第三周期元素形成的简单离子中,半径最小的是Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质,遇到盐酸或强碱溶液都能反应的一组是
A.Cu Al2O3NaHCO3B.Mg Al(OH)3Na2CO3
C.Fe Al2O3Al(OH)3D.Al NaHCO3Al2O3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com