
| A.高温多雨时比较适合施用钾肥 |
| B.长期施用硫铵会造成土壤板结 |
| C.石硫合剂必须与硫酸混合后才能施用 |
| D.草木灰可以和铵态氮肥一块施用 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
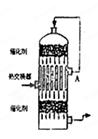
| A.SO2 | B.SO3、O2 | C.SO2、SO3 | D.SO2、O2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.③④⑤⑦ | B.①②⑤⑥ | C.②⑥ | D.②③⑥⑦ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.硫磺和硫铁矿均可作为生产原料 |
| B.将矿石粉碎,是为了提高矿石的利用率 |
| C.反应中通入过量的空气是为了提高FeS2和SO2的转化率 |
| D.从吸收塔出来的硫酸经浓缩后可以变成发烟硫酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.合成氨生产过程中升高温度可加快反应速率,缩短生产周期,故温度越高越好 |
| B.硫酸工业中,使用催化剂是为了提高SO2转化为SO3的转化率 |
| C.电解精炼铜时,精铜作阴极 |
| D.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.化工厂用氯气制漂白粉 | B.冶炼厂用氧化铝生产铝 |
| C.硝酸厂用氨制硝酸 | D.炼油厂分馏法生产汽油 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
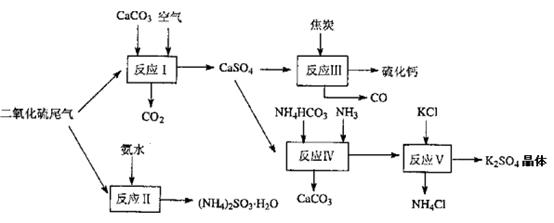
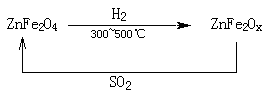
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 H2NCONHSO3H(s) △H<0
H2NCONHSO3H(s) △H<0 2H2NSO3H + CO2↑
2H2NSO3H + CO2↑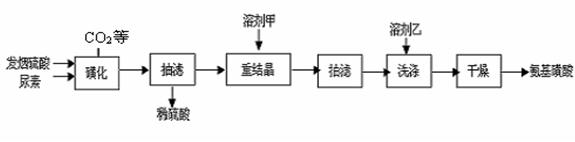

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com