
 某小组为了探究电化学原理,设计了如图所示的电化学装置,电极Ⅰ为锌,其它电极均为石墨,盐桥是浸泡了饱和氯化钾溶液的琼脂,丙池是滴加了酚酞的氯化钠溶液,下列叙述正确的是( )
某小组为了探究电化学原理,设计了如图所示的电化学装置,电极Ⅰ为锌,其它电极均为石墨,盐桥是浸泡了饱和氯化钾溶液的琼脂,丙池是滴加了酚酞的氯化钠溶液,下列叙述正确的是( )| A、电子由电极Ⅳ通过外电路流向电极Ⅰ |
| B、装置工作过程中Ⅲ电极周围出现红色 |
| C、电极Ⅱ发生还原反应 |
| D、盐桥中Cl-向乙池移动 |


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
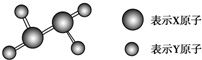 某分子的球棍模型如图所示.已知分子中所有原子的最外层均达到8电子稳定结构,原子间以单键相连.下列有关说法中错误的是( )
某分子的球棍模型如图所示.已知分子中所有原子的最外层均达到8电子稳定结构,原子间以单键相连.下列有关说法中错误的是( )| A、X原子可能为第ⅤA族元素 |
| B、Y原子一定为第ⅠA族元素 |
| C、该分子中,只含有共价键 |
| D、从圆球的大小分析,该分子可能为N2F4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学式 | 电离平衡常数(25℃) |
| HCN | K=4.9×10-10 |
| H2CO3 | K1=4.3×10-7,K2=5.6×10-11 |
| c(HCN) |
| c(CN-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将氨水逐滴滴入AgNO3溶液中,至过量 |
| B、将二氧化碳通入Ca(OH)2 溶液中,至过量 |
| C、将氯气通入AgNO3溶液中好,至过量 |
| D、将二氧化氮通入Ba(OH)2 溶液中,至过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,11.2L Cl2中含有的分子数为0.5NA |
| B、标准状况下,11.2L H2O 中含有的分子数为0.5NA |
| C、64g SO2 中含有的原子数为3NA |
| D、0.5NA O2 物质的量为1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
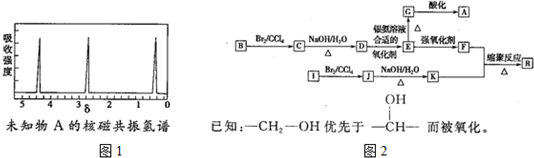
查看答案和解析>>
科目:高中化学 来源: 题型:
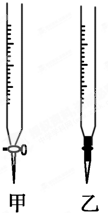 某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,完成以下填空:
某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,完成以下填空:| 滴定次数 | 待测液体积/mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 20 | 1.02 | 21.02 |
| 2 | 20 | 2.00 | 25.00 |
| 3 | 20 | 0.60 | 20.60 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com