
【题目】某羧酸衍生物A,其分子式为C6H12O2 , 实验表明A和氢氧化钠溶液共热生成B和C,B和盐酸反应生成有机物D,C在铜催化和加热的条件下氧化为E,其中D、E都不能发生银镜反应.由此判断A的可能的结构有( )
A.6种
B.2种
C.4种
D.3种
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】下列科研成果不是由我国发明或创造的是( )
A.世界上第一个由人工合成的、具有生理活性的蛋白质﹣﹣结晶牛胰岛素
B.黑火药和造纸
C.发现元素周期律
D.青蒿素的合成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究,其结构简式如图所示.下列关于分枝酸的叙述正确的是( ) 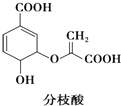
A.分子中含有2种官能团
B.可与乙醇、乙酸反应,且反应类型相同
C.1 mol分枝酸分子中含2mol﹣OH(羟基)
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三代混合动力车目前一般使用镍氢电池(M表示储氢合金;汽车在刹车或下坡时,电池处于充电状态)。镍氢电池充放电原理的示意图如下:

其总反应式为![]() 。根据所给信息判断,下列说法错误的是
。根据所给信息判断,下列说法错误的是
A. 混合动力汽车上坡或加速时,乙电极的电极反应式为:NiOOH+H2O+eˉ==Ni(OH)2+OHˉ
B. 混合动力汽车上坡或加速时,电解液中OHˉ向甲电极移动
C. 混合动力汽车下坡或刹车时,甲电极周围溶液的pH减小
D. 混合动力汽车下坡或刹车时,电流的方向为:甲电极→发动机→乙电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按题给要求填空
(1)写出以乙炔为原料制备聚氯乙烯反应方程式(无机物不限)
① .
② .
(2)分子式为C6H12 的某烃的所有碳原子都在同一平面上,则该烃的结构简式为 , 若分子式为C4H6的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为 .
(3)1分子某烷烃含有50个电子,该烷烃只能由一种结构的炔烃加氢得到,则该烷烃的结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:NOx能与Na2O2反应;NO和NO2均能与酸性KMnO4溶液反应生成NO3ˉ和Mn2+。
I.用下图所示装置(略去夹持仪器)可制得少量亚硝酸钠(2NO+Na2O2=2NaNO2)。

(1)B、D的仪器名称是________,D的作用是________。
(2)通NO前,需先通一段时间N2,目的是________,
(3)E中主要反应的离子方程式为________,
(4)常温下,测得实验前后C的质量差值为0.30g,则制得NaNO2________g。
Ⅱ.NO2和Na2O2都有较强氧化性,为探究NO2与Na2O2反应的产物,提出如下假设:
假设i.NO2氧化Na2O2;假设ii.Na2O2氧化NO2。
甲同学设计如图所示实验装置:

请回答下列问题:
(5)单向阀在实现气体单向流通的同时,还有一个作用是___________。
(6)待试管G中收集满气体,向试管G中加入适量Na2O2粉末,塞紧塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃,甲同学据此认为假设i正确。乙同学认为该装置不能达到实验目的,为达到实验目的,应在F、G之间增加一个M装置,M中应盛装__________(可供选择的试剂:碱石灰,浓硫酸饱和氯化钠溶液);乙同学用改进后的装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失,带火星的木条未复燃。得到结论:假设ⅱ正确。
请做出正确判断,写出NO2和Na2O2反应的化学方程式__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《战争的气体化学和分析》中介绍了一种制取COC12(光气,熔点为-118℃,沸点为8.2℃,微溶于水,易溶于甲苯等有机溶剂)的方法,其实验装置如图所示(夹持装置已省略)。已知:3CCl4+2H2SO4(浓) ![]() 3COCl2↑+4HCl+ S2O5Cl2。下列说法正确的是
3COCl2↑+4HCl+ S2O5Cl2。下列说法正确的是

A. 该反应属于氧化还原反应
B. 自来水从冷凝管的X口通入,且被冷凝的物质是CCl4
C. 可将装置丁的尾气通过导管直接通入NaOH溶液中进行尾气处理
D. 装置乙中可收集到光气的甲苯溶液,装置丙、丁均可收集到液态光气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于阿伏加德罗常数的叙述错误的是
A.物质的量越大,阿伏加德罗常数就越大
B.1mol任何粒子的数目都约等于6.02×1023
C.符号为NA,通常用6.02×1023mol-1表示
D.在数值上等于12g12C中所含的碳原子数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com