

分析 (1)吸收硫酸工业尾气中的二氧化硫,同时制得硫酸铵,吸收塔中通入空气是利用氧气氧化二氧化硫为硫酸盐;
(2)氨气溶于水显碱性,控制氨气的量来控制溶液的酸碱性;
解答 解:(1)依据流程图分析,吸收塔中发生反应是二氧化硫、一水合氧气反应生成硫酸铵和水,反应的化学方程式为:4NH3?H2O+2SO2+O2═2(NH4)2SO4+2H2O;
故答案为:4NH3?H2O+2SO2+O2═2(NH4)2SO4+2H2O;
(2)吸收塔中溶液的pH在5.5~6.0之间,生产效率较高.氨气溶于水显碱性,控制氨气的量来控制溶液的酸碱性,所以当控制一定流量的尾气时,调节溶液的pH的方法是,调节氨水的流量,
故答案为:调节氨水的流量;
点评 本题考查了氨气和二氧化硫的性质,题目难度不大,侧重于基础知识的考查,注意把握反应原理.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 2008年北京残奥会吉祥物是“福牛乐乐”(Fumulele).有一种有机物的键线式也酷似牛.故称为牛式二烯炔醇(eowenynenyno1)
2008年北京残奥会吉祥物是“福牛乐乐”(Fumulele).有一种有机物的键线式也酷似牛.故称为牛式二烯炔醇(eowenynenyno1)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{2}^{3}$He原子核内含有2个中子 | |
| B. | ${\;}_{2}^{3}$He原子核内含有3个质子 | |
| C. | ${\;}_{2}^{3}$He原子核外有3个电子 | |
| D. | ${\;}_{2}^{3}$He和${\;}_{2}^{4}$He是两种不同的核素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 物质(括号中为杂质) | 除杂试剂 | 操作 |
| A | CO2(SO2) | 饱和NaHCO3溶液 | 洗气 |
| B | BaCO3(BaSO4) | 饱和Na2CO3溶液 | 搅拌、过滤 |
| C | 苯(苯酚) | 浓溴水 | 过滤 |
| D | Cl2(HCl) | 饱和食盐水 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
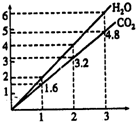 两种气态烃组成的混合气体,完全燃烧后得到C02和H2O的物质的量随着混合烃物质的量的变化如图所示.则下列对混合烃的判断正确的是( )
两种气态烃组成的混合气体,完全燃烧后得到C02和H2O的物质的量随着混合烃物质的量的变化如图所示.则下列对混合烃的判断正确的是( )| A. | 一定含有CH4 | B. | 一定含有C2H6 | C. | 一定含有C2H4 | D. | 一定不含有C3H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:A大于B | B. | A和B可能在同一主族 | ||
| C. | A可能在第2周期ⅣA族 | D. | A肯定是金属元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com