
【题目】氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3 , 请回答下列问题:
①比较Na3N中两种微粒的半径r(Na+)r(N3﹣)(填“>”“<”或“=”),
②Na3N与水反应属于反应(填“氧化还原”或“非氧化还原”);
③Na3N与盐酸反应生成两种盐的化学式为;
④写出化合物Na3N的电子式: .
【答案】<;非氧化还原;NH4Cl、NaCl;![]()
【解析】解:①电子层结构相同的离子,核电荷数越大离子半径越小,故离子半径r(Na+)<r(N3﹣),所以答案是:<;②Na3N与水反应生成NaOH与氨气,元素化合价没有发生变化,属于非氧化还原反应,所以答案是:非氧化还原;③Na3N与盐酸反应生成两种盐为氯化铵与氯化钠,所以答案是:NH4Cl、NaCl;④Na3N属于离子化合物,由钠离子与氮离子构成,电子式为: ![]() ,所以答案是:
,所以答案是: ![]() .
.
【考点精析】解答此题的关键在于理解微粒半径大小的比较的相关知识,掌握同周期元素的原子或最高价离子半径从左到右逐渐减小(稀有气体元素除外);电子层数相同,核电荷数越大半径越小;核电荷数相同,电子数越多半径越大;电子数和核电荷数都不同的,一般通过一种参照物进行比较;具有相同电子层结构的离子,一般是原子序数越大,离子半径越小.


科目:高中化学 来源: 题型:
【题目】化学是你,化学是我,化学深入我们生活,下列说法正确的是
A.木材纤维和土豆淀粉遇碘水均显蓝色
B.食用花生油和鸡蛋清都能发生水解反应
C.包装用材料聚乙烯和聚氯乙烯都属于烃
D.PX项目的主要产品对二甲苯属于饱和烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语使用正确的是( )
A.NH4Cl的电子式: 
B.用电子式表示氯化氢分子的形成过程: ![]()
C.氧化钠的电子式: ![]()
D.R2+离子核外有a个电子,b个中子,R原子表示为: ![]() R
R
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合溶液中含有两种溶质NaCl和H2SO4,且n(NaCl): n(H2SO4)=3:1。若以石墨电极电解该混合液时根据电极产物,可明显分为三个阶段,下列叙述中不正确的是( )
A. 阴极自始至终只析出H2 B. 阳极先析出Cl2,后析出O2
C. 电解最后阶段为电解水 D. 电解液的pH不断增大,最终等于7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,a、b、c、d均为石墨电极,通电进行电解,下列说法正确的是( )
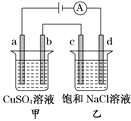
A. 电路中电子流向:负极→d→c→b→a→正极
B. a、c两极产生气体的物质的量相等
C. SO42-向b电极运动,Cl-向c电极运动
D. 通电后乙烧杯滴入酚酞溶液d极会变红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相对分子质量为 M 的气态化合物V L(标准状况),溶于m g 水中, 得到质量分数为 w、物质的量浓度为c mol/L、密度为ρg/mL 的溶液,下列说法正确的是
A. 相对分子质量![]() B. 物质的量浓度
B. 物质的量浓度![]()
C. 溶液的质量分数![]() D. 溶液密度
D. 溶液密度![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,摩托罗拉公司开发了一种以液态甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月.下图是一个电化学过程的示意图.

已知甲池的总反应式为:2CH3OH+3O2+4KOH![]() 2K2CO3+6H2O
2K2CO3+6H2O
请填空:
(1)充电时:①原电池的负极与电源________极相连 ②阳极的电极反应为_________________.
(2)在此过程中若完全反应,乙池中B极的质量增加648g,则甲池中理论上消耗O2_____L(标准状况下).
(3)若在常温常压下,1gCH3OH燃烧生成CO2和液态H2O时放热22.68kJ,表示该反应的热化学方程式为______________________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com