
| A. | 这种口服液含丰富的氮、磷、锌等微量元素 | |
| B. | 这种饮料中不含任何化学物质 | |
| C. | 这种蒸馏水绝对纯净,其中不含任何离子 | |
| D. | 没有水就没有生命 |
分析 A.根据人体内的常量元素和微量元素判断;
B.任何物质都是由化学元素组成的,饮料是由化学物质组成的;
C.水是弱电解质,能电离出离子;
D.根据水的重要性判断.
解答 解:A.氮和磷在人体内属于常量元素,不是微量元素,故A错误;
B.分析此广告的本义,应该是要说饮料中不含化学合成的物质,但由于缺乏基本的化学知识,而误把化学合成物质混淆成化学物质,故B错误;
C.水是弱电解质,能电离出离子,所以蒸馏水中含有离子,故C错误;
D.水是生命之源,人类时刻离不开水,所以人类不能没有水,没有水就没有生命,故D正确.
故选D.
点评 本题考查了原子、分子、离子等基础知识,难度不大,学会用化学知识解释生产、生活现象,学以致用.


 作业辅导系列答案
作业辅导系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2S在反应中既是氧化剂又是还原剂 | |
| B. | 以上反应中转移电子的物质的量为1 mol | |
| C. | 以上参加反应的HNO3中被还原的HNO3为2 mol | |
| D. | 反应中,氧化剂和还原剂的物质的量之比为4:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
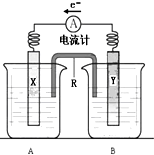 如图是铜锌原电池装置.其电池的总反应是:
如图是铜锌原电池装置.其电池的总反应是:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
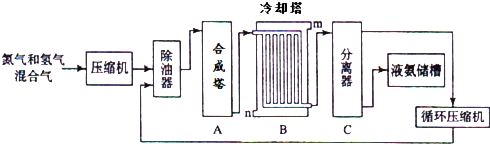
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度,活化分子百分数增大,有效碰撞的几率增大,反应速率增大 | |
| B. | 增大反应物浓度,单位体积内活化分子数增多,有效碰撞的几率增大,反应速率增大 | |
| C. | 具有足够能量的分子相互碰撞就一定能发生化学反应 | |
| D. | 正催化剂能降低反应的活化能,提高活化分子百分数,有效碰撞的几率增大,反应速率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
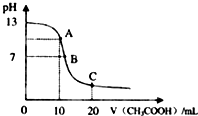 某学生在实验室测定一未知浓度的稀盐酸,已知25℃时,在20ml氢氧化钠标准溶液中逐滴加入0.2mol/L醋酸溶液的PH变化曲线如图所示:
某学生在实验室测定一未知浓度的稀盐酸,已知25℃时,在20ml氢氧化钠标准溶液中逐滴加入0.2mol/L醋酸溶液的PH变化曲线如图所示:| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积 | 19.00 | 21.81 | 21.79 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸的电离方程式:H2CO3?2H++CO32- | |
| B. | 硫化钠水解:S2-+2H2O?H2S+2OH- | |
| C. | 往AgI悬浊液中滴加Na2S饱和溶液:2Ag+ (aq)+S2-(aq)=Ag2S(s) | |
| D. | 用醋酸除水垢:2CH3COOH+CaCO3=2CH3COO-+Ca2++H2O+CO2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com