
在下列所示的微粒中,氧化性最强的是( )
|
| A. | 1S22S22P2 | B. | 1S22S22P5 | C. | 1S22S22P63S1 | D. | 1S22S22P6 |
科目:高中化学 来源: 题型:
下列有关氧化还原反应的叙述中正确的是( )
|
| A. | 化合反应都不是氧化还原反应 |
|
| B. | 氧化还原反应的本质是元素化合价的升降 |
|
| C. | 失电子的反应物在反应中作氧化剂,反应中被还原 |
|
| D. | 金属单质在化学反应中一定做还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
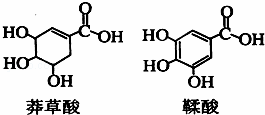
莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )
|
| A. | 两种酸都能与溴水反应 |
|
| B. | 两种酸遇三氯化铁溶液都显色 |
|
| C. | 鞣酸分子与莽草酸分子相比多了两个碳碳双键 |
|
| D. | 等物质的量的两种酸与足量碳酸钠反应消耗碳酸钠物质的量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列基态原子与离子的电子排布式错误的是( )
|
| A. | K:1s22s22p63s23p64s1 |
|
| B. | F﹣:1s22s22p6 |
|
| C. | Fe:1s22s22p63s23p63d54s2 |
|
| D. | Kr:1s22s22p63s23p63d104s24p6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某药物结构简式如图,该物质1mol与足量NaOH溶液反应,消耗的NaOH物质的量为( )
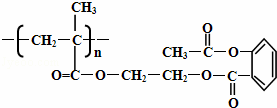
|
| A. | 3mol | B. | 4mol | C. | 3n mol | D. | 4n mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.Na2O、Mn2O7、Fe2O3均为碱性氧化物
B.烧碱不是碱、石炭酸不是酸、双氧水不是水
C.电解质在水溶液中的反应都是离子反应
D.单质都有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
2014年7月1日起,国家卫计委决定禁止使用硫酸铝、硫酸铝钾、硫酸铝铵等含铝元素的物质作为馒头、发糕等膨化食品添加剂。目前使用的无铝泡打粉的成分为小苏打、磷酸二氢钠、碳酸钙等。回答下列问题:
(1)长期食用含铝元素的食品,铝元素会在体内积累,造成毒害。有一泡打粉样品,判断是否含铝元素的实验方法是:________________________________________。
(2)写出磷酸二氢钠在水中的电离方程式:________________________________。
(3)磷酸二氢钠制备流程如下: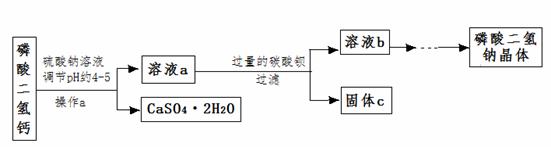
①写出磷酸二氢钙与硫酸钠溶液反应的离子方程式:________________________
②操作a的名称为:_______________,固体c的成份为:___________________
在进行操作a前需控制pH约4-5,若pH过高,得到的产物中可能有:_________
_______(填化学式)
③实验时取46.8g磷酸二氢钙,最终得到59.3g NaH2PO4·2H2O,该实验的产率是:_______
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A. Fe分别与氯气和稀盐酸反应所得氯化物相同
B.K、Zn分别与不足量的稀硫酸反应所得溶液均呈中性
C. Li、Na、K的原子半价和密度随原子序数的增加而增大
D.C、P、S、Cl的最高价氧化物对应水化物的酸性逐渐增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com