
| ������ | Ag+��Na+ |
| ������ | NO3-��SO42-��Cl- |
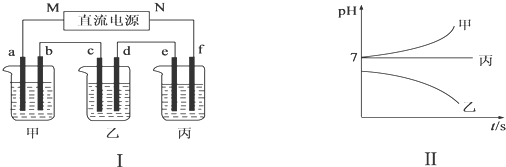
���� �������֪��A��B��C����ǿ����ʣ�������ֻ�ܺ�����������γɿ��������ʣ������������Һ����Һ��Ϊ���ԣ�pH��С����ͼ���п�֪��B����������Һ��������ҺPH�����Ȼ��������������ƣ���AΪ�Ȼ��ƣ���C�������ƣ�
��1��c�缫����������27g����cΪ��������MΪ������NΪ������
��2��n��Ag��=$\frac{27g}{108g/mol}$=0.25mol��ת�Ƶ�����Ϊ0.25mol��f��������Ӧ�缫��ӦʽΪ��4OH--4e-=2H2O+O2�����ݴ˼������������������
��3��b�缫��������ʧȥ���ӷ���������Ӧ�������������ձ������������Һ�����������������
��4�����ݵ����PԪ�غ������غ������
��� �⣺�������֪��A��B��C����ǿ����ʣ�������ֻ�ܺ�����������γɿ��������ʣ������������Һ����Һ��Ϊ���ԣ�pH��С����ͼ���п�֪��B����������Һ��������ҺPH�����Ȼ��������������ƣ���AΪ�Ȼ��ƣ���C�������ƣ�
��1��c�缫����������27g����cΪ��������MΪ������NΪ��������������������������������������������������������c����A���Ȼ��ƣ�
�ʴ�Ϊ������c��NaCl��
��2��n��Ag��=$\frac{27g}{108g/mol}$=0.25mol��ת�Ƶ�����Ϊ0.25mol��f��������Ӧ�缫��ӦʽΪ��4OH--4e-=2H2O+O2�������ݵ�ʧ�����غ㣬��֪�������������ʵ���Ϊ0.25mol��$\frac{1}{4}$=0.0625mol����������Ϊ22.4L/mol��0.625mol=1.4L��
�ʴ�Ϊ��1.4L��
��3��b�缫��������ʧȥ���ӷ���������Ӧ�����������缫��ӦʽΪ��2Cl--2e-=Cl2�������ձ������������Һ�����������������ᣬ��ⷽ��ʽ��4AgNO3+2H2O$\frac{\underline{\;���\;}}{\;}$4Ag+O2��+4HNO3��
�ʴ�Ϊ��2Cl--2e-=Cl2����4AgNO3+2H2O$\frac{\underline{\;���\;}}{\;}$4Ag+O2��+4HNO3��
��4����Ϊ��������Һ���缫��������Һʵ�ʵ��ˮ��c�缫����������27g��ת��0.25mol���ӣ����ݴ�����·
�ص㣬�����缫��ת�Ƶ�������ȣ���
2H2O=H2��+O2����4e-
36g 4mol
m 0.25mol
36g��m=4mol��0.25mol
���m=2.25g��
����Ҫʹ���ָ���ԭ����״̬��Ӧ����ˮ2.25g��
�ʴ�Ϊ��2.25g��
���� ���⿼���˵��ԭ������Ϥ���ع���ԭ��ȷ�жϵ缫�������缫�ķ�����Ӧ�ǽ���ؼ�����Ŀ�Ѷ��еȣ�


 ������ĩ��ϰ��ѵ��ϵ�д�
������ĩ��ϰ��ѵ��ϵ�д� С��ʿ��ĩ����100��ϵ�д�
С��ʿ��ĩ����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �˵���ܷ�����ɫ���� | |
| B�� | H2������O2���� | |
| C�� | ����ʱ���������Һ��pH���ϼ�С | |
| D�� | �缫��Ӧ�ֱ�Ϊ������2H2+4 OH--4e-=4 H2O��������O2+2 H2O+4e-=4 OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | �缫���� | �������Һ | ������ָ��ƫת���� |
| 1 | Mg��Al | ϡ���� | ƫ��Al |
| 2 | Al��Cu | ϡ���� | ƫ��Cu |
| 3 | Al��ʯī | ϡ���� | ƫ��ʯī |
| 4 | Mg��Al | NaOH��Һ | ƫ��Mg |
| 5 | Al�� Cu | Ũ���� | ƫ��Al |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ƿ����Һ©�����ζ�����ʹ�ø�ǰ����Ҫ�����Ƿ�©ˮ����������ͬ�ķ�������Ƿ�©ˮ | |
| B�� | ��Һ��������ʱ��������Һ��������ܳ����ݻ���1/2 | |
| C�� | ǿ��ζ�ǿ��ʱ���÷�ָ̪ʾ�����ü��ȸ����жϵζ��յ� | |
| D�� | ���ʵķ����ᴿ����֮һΪ��ɸ�֡����罺��һ��Ĥ�������ᴿ������Һһ���˷��룬�����Ͼ���������������ӵ�ֱ����Сѡ����к��ʿ��ġ�ɸ�ӡ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӿ�����ֻ���ڷǼ��Թ��ۼ� | |
| B�� | ����?����ˮ�����ɼ��Լ���϶��ɵļ��Է��� | |
| C�� | ����������۵�һ����ԭ�Ӿ���ͣ��ȷ��Ӿ���� | |
| D�� | H2O�ķе��H2S�ߣ�����ΪH2O���Ӽ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| Ԫ�ش��� | L | M | Q | R | T |
| ԭ�Ӱ뾶/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| ��Ҫ���ϼ� | +2 | +3 | +2 | +6��-2 | -2 |
| A�� | �⻯��Ļ�ԭ��ΪH2T��H2R | |
| B�� | ������ϡ���ᷴӦ������ΪL��Q | |
| C�� | L��M��R������������ˮ��������֮����ܷ�Ӧ | |
| D�� | ���Ӱ뾶��L2+��R2- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��μ��백ˮ�У�������Һ��c��H+�������� | |
| B�� | ����ͨ�����C12���١��ھ������ƶ�����ҺpH��С | |
| C�� | ����CaCO3����Һ�У�CaCO3���ܽ�ƽ�������ƶ� | |
| D�� | ����һ����NaOH��Һ�У�������Һ������Ũ�ȵĹ�ϵ����Ϊc��Cl-��+c��ClO-��=c��Na+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
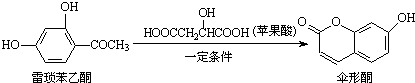
| A�� | ��������ͪ����̼ԭ�Ӳ����ܹ�ƽ�� | |
| B�� | ��������ͪ��ɡ��ͪ���ܸ�FeCl3��Һ������ɫ��Ӧ | |
| C�� | 1 mol��������ͪ������H2��Ӧ���������3 mol H2 | |
| D�� | 1 molɡ��ͪ������NaOH��Һ��Ӧ���������3 mol NaOH |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com