
根据下列事实:①X+Y2+=X2++Y;②Z+H2O(冷)=Z(OH)2+H2↑;③Z2+氧化性比X2+弱;④由Y、W电极组成的电池,电极反应为W2++2e-=W、Y-2e-=Y2+,可知X、Y、Z、W的还原性由强到弱的顺序为
A. X > Z > Y > W B. Z > W > X > Y
C. Z > Y > X > W D. Z > X > Y > W
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
为了完成教材上的“中和热的测定”这个实验
(1)实验桌上有烧杯(大、小两个)、泡沫塑料、泡沫塑料板(中心有两个小孔)、环形玻璃搅拌棒,0.50mol·L-1盐酸、0.55mol·L—1NaOH溶液,尚缺少的实验用品是 。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?答: (填“能”或“否”)。其原因是 。
(3)实验时所用盐酸及NaOH溶液的体积均为50mL,各溶液密度为1g·cm—3,生成溶液的比热容c=4.18J/(g·℃),实验起始温度为t1℃,终止温度为t2℃。试推断中和热的计算式: 。
(4)如果用50mL的0.60mol·L-1盐酸与50mL 的0.55mol·L—1NaOH溶液进行反应。若热量无损失,与上述实验相比,所求中和热 (填“偏大、偏小、相等”),简述理由 。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室制备硝基苯的方法是将苯与浓硫酸和浓硝酸的混合液加热到55~60 ℃反应,已知苯与硝基苯的基本物理性质如下表所示:
| 熔点 | 沸点 | 状态 | |
| 苯 | 5.51 ℃ | 80.1 ℃ | 液体 |
| 硝基苯 | 5.7 ℃ | 210.9 ℃ | 液体 |
(1)要配制浓硫酸和浓硝酸的混合酸的注意事项是___________________ ________________________________________________。
(2)分离硝基苯和水的混合物的方法是 ;分离硝基苯和苯的方法是__________________________________________________。
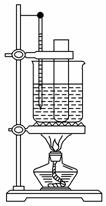
(3)某同学用如图装置制取硝基苯:
①用水浴加热的优点是__________________________________________;
②指出该装置的两处缺陷____________________________________________________;
___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是短元素周期表的一部分,① ~⑨ 是元素周期表中的部分元素。
| ⅠA | 0 | |||||||
| ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| …… | ② | ③ | ④ | |||||
| ⑤ | ⑥ | …… | ⑦ | ⑧ | ⑨ |
请回答下列问题:
(1)元素③④⑧的气态氢化物中最稳定的是 (填化学式)。
(2)元素⑤和⑦的最高价氧化物对应的水化物发生反应的离子方程式是 。
(3)元素⑥和⑨形成的化合物的电子式是 。
(4)③、⑤、⑥形成的简单离子半径由大到小的顺序为 (写离子符号)
(5)由表中两种元素形成的氢化物A和B都含有18个电子,A是一种6原子分子,可做火箭发动机燃料;B是一种常见强氧化剂。已知液态A与液态B充分反应生成一种液态10电子分子和一种气态单质,写出A与B反应的化学方程式: 。
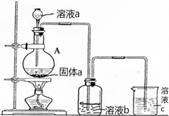 (6)某同学为了比较元素⑧和⑨非金属性的相对强弱,用如图所示装置进行实验:
(6)某同学为了比较元素⑧和⑨非金属性的相对强弱,用如图所示装置进行实验:
①浓溶液a和溶液b分别为 、 (写化学式)。
②浓溶液a与黑色固体a反应的离子方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示的原电池装置,下列说法不正确的是:
A.该装置的能量转化形式为:化学能转化为电能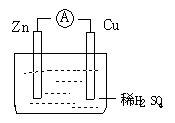
B.电子由Zn片经过导线流向铜片
C.Zn为负极发生还原反应
D.Cu为正极,在Cu片上有气泡产生
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组中化合物的性质比较,不正确的是
A.酸性:HClO4>HBrO4>HIO4
B.碱性:NaOH>Mg(OH)2>Al(OH)3
C.稳定性:PH3>H2S> HCl
D.非金属性:F>O>S
查看答案和解析>>
科目:高中化学 来源: 题型:
现有a—h8种短周期元素,它们在元素周期表中的位置如下所示,据此回答问题 :
| a | |||||||||||||||||
| d | e | ||||||||||||||||
| b | c | f | g | h | |||||||||||||
(1)下列元素原子间容易形成离子键的是_______,化学式为__________。 容易形成共价键的是_________,化学式为_________。
A.C和f B.b和h
C.d和h D.b和e
(2)下列分子中所有原子都满足最外层8电子结构的是________
A.ea3 B.bh
C.fh3 D.dh4
(3)均由a、b、g和氧元素形成的两种离子化合物,其中有一物质相对分子质量为120,该化合物融化时破坏的是__________,电离方程式为__________;溶于水时破坏的是__________,电离方程式为__________。均由a、b、g和氧元素形成的该两种离子化合物,相互反应可生成有刺激性气味的气体,则反应的离子方程式为________。(写在电离方程式下一行)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列图示与对应的叙述相符的是( )
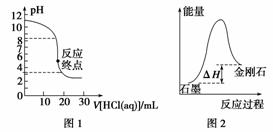
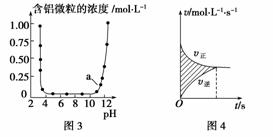
A.图1表示0.001 mol·L-1盐酸滴定0.001 mol·L-1 NaOH溶液的滴定曲线
B.图2表示从能量角度考虑,石墨比金刚石稳定
C.图3表示的是Al3+与OH-反应时含铝微粒浓度变化曲线,图中a点溶液中大量存在Al3+
D.图4所示图中的阴影部分面积的含义是(v正-v逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
CPAE是蜂胶的主要活性成分,它可由咖啡酸合成,其合成过程如下。下列说法不正确的是 ( )
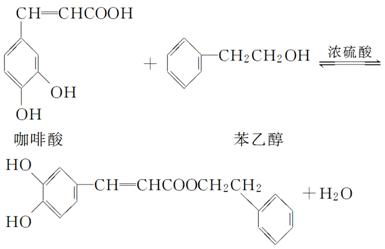
CPAE
A.1 mol CPAE与足量的NaOH溶液反应,最多消耗3 mol NaOH
B.可用金属Na检测上述反应结束后是否残留苯乙醇
C.与苯乙醇互为同分异构体的酚类物质共有9种
D.咖啡酸可发生聚合反应,并且其分子中含有3种官能团
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com