
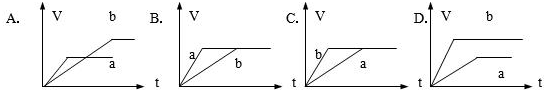
分析 (1)等质量的两份锌粉a、b,分别加入过量的稀H2SO4中,同时向a中放入少量的CuSO4溶液,发生:Fe+Cu2+=Fe2++Cu,形成原电池,反应速率增大,但生成的氢气少;
(2)反应均发生Zn+2H+═Zn2++H2↑,Zn过量,则相同体积、相同物质的量浓度的稀硫酸完全反应,生成氢气相同,且a中加入少量硫酸铜溶液,构成Cu、Zn原电池,加快反应的速率,以此来解答;
(3)向a中放入少量的醋酸钠溶液,则醋酸钠和硫酸反应生成醋酸和硫酸钠,酸性减弱,但是氢离子的物质的量不变.
解答 解:(1)等质量的两份锌粉a、b,分别加入过量的稀H2SO4中,同时向a中放入少量的CuSO4溶液,发生的反应为:Zn+Cu2+=Zn2++Cu,铜-铁-稀硫酸形成原电池,反应速率增大,反应用时少于b,但生成的氢气少也少于b,图象应为A,
故答案为:A;
(2)由题意可知,反应均发生Zn+2H+═Zn2++H2↑,Zn过量,则相同体积、相同物质的量浓度的稀硫酸完全反应,生成氢气相同,
且a中加入少量硫酸铜溶液,构成Cu、Zn原电池,加快反应的速率,所以a反应速率快,达到反应结束时的时间短,显然只有B图象符合,
故答案为:B;
(3)等质量的两份锌粉a、b,分别加入过量的稀H2SO4中,同时向a中放入少量的醋酸钠溶液,则醋酸钠和硫酸反应生成醋酸和硫酸钠,酸性减弱,所以速率减慢,但是氢离子的物质的量不变,所以反应产生氢气的量不变,故答案为:C.
点评 本题考查了根据图象判断反应速率的大小,难度不大,分析图象时注意图象的拐点及走向和变化趋势.


科目:高中化学 来源: 题型:选择题
| A. | 氯气、液氯和氯水是同一种物质 | |
| B. | Na2O、Na2O2组成元素相同,与CO2都能发生氧化还原反应 | |
| C. | 硫酸钡难溶于水,但硫酸钡是电解质 | |
| D. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
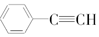 与C8H6互为同分异构体.
与C8H6互为同分异构体.| A. | ①③ | B. | ①②④ | C. | ③④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅晶体是由SiO2分子构成的,它的熔点低、硬度大 | |
| B. | 由SiO2不能与水反应生成H2SiO3,可知SiO2不是H2SiO3的酸酐 | |
| C. | 将硫酸和碳酸钠反应产生的气体通入Na2SiO3溶液产生白色沉淀,可知酸性H2CO3>H2SiO3 | |
| D. | SiO2既能与NaOH溶液反应又能与氢氟酸反应,所以SiO2是两性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
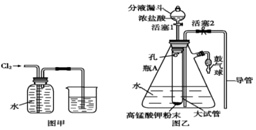 氯水是实验室常需临时配制的一种试剂,图甲所示的是实验室配制氯水时的一种常用装置,图乙是某化学实验小组自行设计的一种配制氯水的装置(图中的鼓气球是一种具有气体单向阀的、可用于向瓶中鼓入空气的仪器).
氯水是实验室常需临时配制的一种试剂,图甲所示的是实验室配制氯水时的一种常用装置,图乙是某化学实验小组自行设计的一种配制氯水的装置(图中的鼓气球是一种具有气体单向阀的、可用于向瓶中鼓入空气的仪器).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同状况下两电极上产生的气体体积之比为2:1 | |
| B. | 两电极上产生的气体质量之比为8:1 | |
| C. | 相同状况下两电极上产生的气体体积之比为4:1 | |
| D. | 若两电极上产生的气体质量比为16:3,则D2O与H2O的物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com