
分析 (1)pH=1的混合溶液中c(H+)=0.1mol/L,混合溶液中c(H+)=$\frac{0.15×2×{V}_{1}-0.1×{V}_{2}}{{V}_{1}+{V}_{2}}$mol/L=0.1mol/L,据此计算V1:V2;
(2)①若由0.1mol•L-1 HA溶液与0.1mol•L-1 NaOH溶液等体积混合而得,如果HA是弱酸,二者恰好反应生成强碱弱酸盐,溶液呈碱性,如果酸是强酸,二者恰好反应生成强酸强碱盐,溶液呈中性;
②若溶液pH>7,说明c(H+)<c(OH-),根据电荷守恒判断c(Na+)、c(A-)相对大小;
(3)根据c(酸)=$\frac{c(碱)×V(碱)}{V(碱)}$判断不当操作对相关物理量的影响
解答 解:(1)pH=1的混合溶液中c(H+)=0.1mol/L,混合溶液中c(H+)=$\frac{0.15×2×{V}_{1}-0.1×{V}_{2}}{{V}_{1}+{V}_{2}}$mol/L=0.1mol/L,整理可得:V1:V2=1:1,
故答案为:1:1;
(2)①若由0.1mol•L-1 HA溶液与0.1mol•L-1 NaOH溶液等体积混合而得,如果HA是弱酸,二者恰好反应生成强碱弱酸盐,溶液呈碱性,则pH>7,如果酸是强酸,二者恰好反应生成强酸强碱盐,溶液呈中性,所以pH=7,
故答案为:≥;
②若溶液pH>7,说明c(H+)<c(OH-),根据电荷守恒c(H+)+c(Na+)=c(OH-)+c(A-)可知:c(Na+)>c(A-),
故答案为:>;根据电荷守恒,c(H+)+c(Na+)=c(OH-)+c(A-),由于c(OH-)>c(H+),故c(Na+)>c(A-);
(3)A.滴定终点读数时,俯视滴定管的刻度,V(碱)偏小,根据c(酸)=$\frac{c(碱)×V(碱)}{V(碱)}$可知c(酸)偏小,故A错误;
B.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗,待测液的物质的量不变,则V(碱)不变,根据c(酸)=$\frac{c(碱)×V(碱)}{V(碱)}$可知c(酸)不变,故B错误;
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液,造成V(碱)偏高,根据c(酸)=$\frac{c(碱)×V(碱)}{V(碱)}$可知c(酸)偏高,故C正确;
D.未用标准液润洗碱式滴定管,标准液碱的浓度偏小,造成V(碱)偏高,根据c(酸)=$\frac{c(碱)×V(碱)}{V(碱)}$可知c(酸)偏高,故D正确;
故答案为:CD.
点评 本题考查了酸碱混合的定性判断及溶液pH的计算、离子浓度大小比较及中和滴定中的误差分析等知识,题目难度中等,明确溶液酸碱性与溶液pH的关系为解答关键,注意掌握中和滴定操作方法,能够根据盐的水解原理、电荷守恒等知识正确判断离子浓度大小,试题培养了学生的分析能力及灵活应用能力.


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.25(b-2a)mol/L | B. | 4(2a-b)mol/L | C. | 2(b-2a)mol/L | D. | 4(b-2a)mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
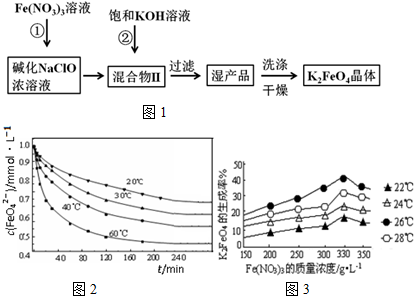
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴水和淀粉溶液 | B. | AgNO3溶液和稀硝酸 | ||
| C. | CCl4溶液 | D. | 氯水和碘化钾淀粉溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同.打开活塞,使NO与O2充分反应(2NO+O2=2NO2).(不考虑NO2与N2O4的转化)
如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同.打开活塞,使NO与O2充分反应(2NO+O2=2NO2).(不考虑NO2与N2O4的转化)查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X>Y>Z | B. | Y>Z>X | C. | X>Z>Y | D. | Z>X>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考如图所示仪器从表中选出正确选项( )
用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考如图所示仪器从表中选出正确选项( ) | 选项 | 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 |
| A | 碱 | 酸 | 石蕊 | 乙 |
| B | 酸 | 碱 | 酚酞 | 甲 |
| C | 碱 | 酸 | 甲基橙 | 乙 |
| D | 酸 | 碱 | 酚酞 | 乙 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③ | C. | ③④ | D. | ①② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com