
碳、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用。
(1)真空碳热还原—氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
2Al2O3(s)+2AlCl3(g)+6C(s)=6AlCl(g)+6CO(g) △H=a kJ·mol-1
3AlCl(g) =2Al(l)+AlCl3(g) △H=b kJ·mol-1
反应Al2O3(s)+3C(s)=2Al(l)+3CO(g)的△H= kJ·mol-1(用含a、b的代数式表示);
(2)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g) N2(g)+CO2(g) △H="Q" kJ·mol-1。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g) △H="Q" kJ·mol-1。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
| 时间(min) 浓度(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |

(15分)(1)0.5a+b(2分) (2)①0.032mol·L-1·min-1(1分), 0.25 (2分);
② ad(2分,选对一个给1分,错选不给分); ③<(2分);
④bc(2分,选对一个给1分,错选不给分);(3)Ag 2O+2e-+H2O=2Ag+2OH-(2分); 2(2分)
解析试题分析:(1)根据反应①2Al2O3(s)+2AlCl3(g)+6C(s)=6AlCl(g)+6CO(g) △H=a kJ·mol-1、②3AlCl(g) =2Al(l)+AlCl3(g) △H=b kJ·mol-1并依据盖斯定律可知,①÷2+②即得到反应A Al2O3(s)+3C(s)=2Al(l)+3CO(g),所以该反应的△H=(0.5a+b)KJ/mol。
(2)①根据表中数据可知,0~10min内,NO的平均反应速率v(NO)= =0.032mol?L-1?min-1;根据表中数据可知,反应C(s)+2NO(g)
=0.032mol?L-1?min-1;根据表中数据可知,反应C(s)+2NO(g) N2(g)+CO2(g)的平衡浓度c(N2)=0.25mol/L;c(CO2)=0.25mol/L;c(NO)=0.5mol/L,所以该反应的平衡常数K=
N2(g)+CO2(g)的平衡浓度c(N2)=0.25mol/L;c(CO2)=0.25mol/L;c(NO)=0.5mol/L,所以该反应的平衡常数K=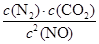 =
=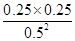 =0.25。
=0.25。
②30min后,只改变某一条件,反应C(s)+2NO(g) N2(g)+CO2(g)重新达到平衡。依据图表数据分析,平衡状态物质浓度增大,依据平衡常数计算K=
N2(g)+CO2(g)重新达到平衡。依据图表数据分析,平衡状态物质浓度增大,依据平衡常数计算K=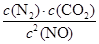 =
=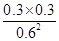 =0.25。由于平衡常数随温度变化,平衡常数不变说明改变的条件一定不是温度;依据数据分析,氮气浓度增大,二氧化碳和一氧化氮浓度增大,反应前后气体体积不变,所以可能是减小容器体积后加入一定量一氧化氮。
=0.25。由于平衡常数随温度变化,平衡常数不变说明改变的条件一定不是温度;依据数据分析,氮气浓度增大,二氧化碳和一氧化氮浓度增大,反应前后气体体积不变,所以可能是减小容器体积后加入一定量一氧化氮。
a.通入一定量的NO,新平衡状态下物质平衡浓度增大,故a正确;
b.加入一定量的活性炭,碳是固体对平衡无影响,平衡不动,故b错误;
c.加入合适的催化剂,催化剂只改变化学反应速率,不改变化学平衡,故C错误;
d.适当缩小容器的体积,反应前后体积不变,平衡状态物质浓度增大,故d;
因此正确的答案为ad。
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为3:1:1,这说明升高温度平衡向逆反应方向移动,因此逆反应是吸热反应,则正反应是放热反应,故Q<0。
④在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。恒容条件下,体积不变。
a、无论反应是否达到平衡状态,单位时间内生成2n mol NO(g)的同时消耗n mol CO2(g),故a错误;
b、该反应是放热反应,所以反应体系的温度随着反应的移动而改变,当平衡时,反应体系的温度不变,故b正确;
C、密度是混合气的质量和容器容积的比值,反应中有固体参加,反应前后气体的质量不等,所以当反应达到平衡时,混合气体的密度不再变化,故c正确;
d、反应前后体积不变,所以无论反应是否达到平衡状态,压强始终不变,故d错误,答案选bc。
(3)原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。所以根据装置图可知,负极是铝,失去电子。正极上氧化银得电子和水反应生成银和氢氧根离子,电极反应式为Ag 2O+2e-+H2O=2Ag+2OH-;根据反应中得失电子数相等计算,消耗27mg Al失去电子是 ×3=0.003mol。所以根据反应式2CuSO4+2H2O
×3=0.003mol。所以根据反应式2CuSO4+2H2O 2Cu+2H2SO4+O2↑可知,反应中生成氢离子的物质的量=0.003mol,所以溶液中氢离子物质的量的浓度=0.003mol÷0.3L=0.01mol/L,所以pH=-lg0.01=2。
2Cu+2H2SO4+O2↑可知,反应中生成氢离子的物质的量=0.003mol,所以溶液中氢离子物质的量的浓度=0.003mol÷0.3L=0.01mol/L,所以pH=-lg0.01=2。
考点:考查反应热、反应速率和平衡常数的计算;外界条件对平衡状态的影响以及平衡状态的判断;电化学原理的有关应用以及pH的有关计算等


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:问答题
(18分)为有效控制雾霾,各地积极采取措施改善大气质量,研究并有效控制空气中的氮氧化物、碳氧化物和硫氧化物含量显得尤为重要。
(1)汽车内燃机工作时会引起N2和O2的反应:N2(g)+O2(g) 2NO(g),是导致汽车尾气中含有NO的原因之一。
2NO(g),是导致汽车尾气中含有NO的原因之一。
①在T1、T2温度下,一定量的NO发生分解反应时N2的体积分数随时间变化如图所示,根据图像判断反应N2(g)+O2(g) 2NO(g)的△H__________0(填“>”或“<”)。
2NO(g)的△H__________0(填“>”或“<”)。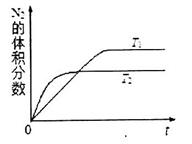
②在T3温度下,向2L密闭容器中充入10molN2与5mo1O2,50秒后达到平衡,测得NO的物质的量为2mol,则该反应的速率v (N2)=___________________。该温度下,若开始时向上述容器中充入N2与O2均为1 mol,则达到平衡后N2的转化率为____________。
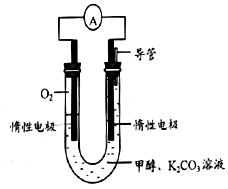
(2)利用下图所示装置(电极均为惰性电极)可吸收SO2,用阴极排出的溶液可吸收NO2。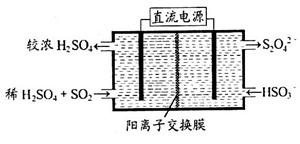
①阳极的电极反应式为_____________________。
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO32—生成。该反应中氧化剂与还原剂的物质的量之比为_______________。
(3)一定条件下可用甲醇与CO反应生成醋酸消除CO污染。常温下,将a mol·L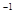 的醋酸与b mol
的醋酸与b mol L
L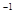 Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=______________________(用含a和b的代数式表示)。
Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=______________________(用含a和b的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
I.800℃时,向容积为2L的恒容密闭容器中充入一定量的CO和H2O维持恒温,发生反应CO(g)+H2O(g) H2(g)+CO2(g),反应过???中测定的部分数据见下表:
H2(g)+CO2(g),反应过???中测定的部分数据见下表:
| 反应时间/min | 0 | 2 | 4 | 6 |
| n(CO)/mol | 1.20 | 0.90 | | 0.80 |
| n(H2O)/ mol | 0.60 | | 0.20 | |


 2NH4+(aq) + Mg(OH)2(s)该反应化学平衡常数的表达式为K= ,列出该反应平衡常数K与Kb(NH3·H2O)、Ksp(Mg(OH)2)的关系式 。
2NH4+(aq) + Mg(OH)2(s)该反应化学平衡常数的表达式为K= ,列出该反应平衡常数K与Kb(NH3·H2O)、Ksp(Mg(OH)2)的关系式 。查看答案和解析>>
科目:高中化学 来源: 题型:计算题
在密闭容器中将NO2加热到某温度时,进行如下的反应:2NO2 2NO+O2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NO2)=0.06 mol/L,c(NO)=0.24 mol/L。试求:
2NO+O2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NO2)=0.06 mol/L,c(NO)=0.24 mol/L。试求:
(1)NO2的转化率为多少?
(2)反应前后的压强比为多少?
(3)计算该温度下反应的平衡常数.
(4)在这5分钟内,用O2来表示的平均反应速率是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图。反应在t时到达平衡,依图所示:
①该反应的化学方程式是 。
②反应起始至t,Y的平均反应速率是 。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
某温度下,在一固定容积的密闭容器中投入一定物质的量的N2与H2进行可逆反应:N2(g)+3H2(g)  2NH3(g) 在2 min时达到平衡状态,此时c(N2)=5.00 mol/L,c(H2)=10.00mol/L,c(NH3)=5.00 mol/L。试求:(写出解题过程)
2NH3(g) 在2 min时达到平衡状态,此时c(N2)=5.00 mol/L,c(H2)=10.00mol/L,c(NH3)=5.00 mol/L。试求:(写出解题过程)
(1)该温度下,反应的平衡常数是多少?
(2)H2的起始浓度;
(3)用N2表示该反应的反应速率是多少;
(4)N2的转化率(保留三位有效数字);
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
(1)将不同量的CO(g)和H2O(g)分别通入体积2L的恒容密闭容器中,进行反应CO(g)+H2O(g) CO2(g)+H2(g),得到如下两组数据:
CO2(g)+H2(g),得到如下两组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |

查看答案和解析>>
科目:高中化学 来源: 题型:计算题
(1)N2(g)+3H2(g) 2NH3(g) △H=-94.4kJ·mol-1。恒容时,体系中各物质浓度随时间变化的曲线如图示。
2NH3(g) △H=-94.4kJ·mol-1。恒容时,体系中各物质浓度随时间变化的曲线如图示。
①在1L容器中发生反应,前20min内,v(NH3)= ,放出的热量为 ;
②25min时采取的措施是 ;
③时段III条件下,反应的平衡常数表达式为 (用具体数据表示)。
(2)电厂烟气脱氮的主反应①:4NH3(g)+6NO(g) 5N2(g)+6H2O(g) △H<0,副反应②:2NH3(g)+8NO(g)
5N2(g)+6H2O(g) △H<0,副反应②:2NH3(g)+8NO(g) 5N2O(g)+3H2O(g) △H>0。平衡混合气中N2与N2O含量与温度的关系如右图。请回答:在400K~600K时,平衡混合气中N2含量随温度的变化规律是 ,导致这种规律的原因是 (任答合理的一条原因)。
5N2O(g)+3H2O(g) △H>0。平衡混合气中N2与N2O含量与温度的关系如右图。请回答:在400K~600K时,平衡混合气中N2含量随温度的变化规律是 ,导致这种规律的原因是 (任答合理的一条原因)。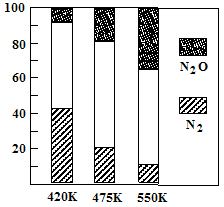
(3)直接供氨式燃料电池是以NaOH溶液为电解质的。电池反应为:4NH3+3O2=2N2+6H2O,则负极电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(1)Zn粒和稀盐酸反应一段时间后,反应速率会减慢,当加热或加入浓盐酸后,反应速率明显加快。由此判断,影响化学反应速率的因素有 和 。
(2)为探究锌与盐酸反应过程的速率变化,某同学的实验测定方法是:在100ml稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(氢气体积已换算为标准状况):
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 体积/mL | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com