
| A. | X可以发生加成反应 | |
| B. | 等物质的量的乙醇、X完全燃烧,消耗氧气的量不相同 | |
| C. | 步骤②需要在氢氧化钠醇溶液中反应 | |
| D. | 步骤①的反应类型是水解反应 |
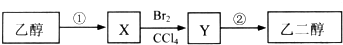
分析 由乙醇合成乙二醇的路线为乙醇发生消去反应生成乙烯,乙烯与溴发生加成生成二溴乙烷,二溴乙烷水解生成乙二醇,所以X为乙烯,Y为BrCH2CH2Br,根据CH3CH2OH和HOCH2CH2OH的分子式即可判断出它们消耗氧气的物质的量,以此解答该题.
解答 解:乙醇发生消去反应生成乙烯,乙烯与溴发生加成生成1,2-二溴乙烷,1,2-溴乙烷水解生成乙二醇.因此X为乙烯,Y为1,2-二溴乙烷.
A.X为乙烯,含有碳碳双键,能够发生加成反应,故A正确;
B.乙醇燃烧耗氧部分为C2H4,因此等物质的量的乙醇、X完全燃烧,消耗氧气的量相同,故B错误;
C.步骤②为1,2-溴乙烷水解生成乙二醇,反应条件为氢氧化钠水溶液,故C错误;
D.步骤①为乙醇发生消去反应生成乙烯,故D错误.
故选A.
点评 本题以有机物的合成考查有机物的结构与性质,题目难度不大,掌握乙醇和卤代烃的性质是解题的关键,答题时注意有机基础知识的灵活运用.


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 聚丙烯塑料的结构简式为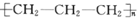 | |
| B. | 聚氯乙烯塑料单体的电子式为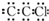 | |
| C. | 塑料购物袋的生产原料需要消耗大量木材 | |
| D. | 聚乙烯中含碳质量分数与其单体的含碳质量分数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 完成下列小题
完成下列小题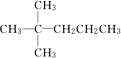 ,
,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
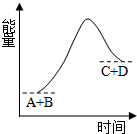
| A. | 形成C、D键释放的总能量大于断A、B键吸收的总能量 | |
| B. | 此反应反应物的总能量高于生成物的总能量 | |
| C. | 此反应为一个吸热的反应 | |
| D. | 此反应只有在加热条件下才能进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2•8H2O与NH4Cl反应 | B. | 铝与稀盐酸 | ||
| C. | 灼热的炭与CO2反应 | D. | 氢氧化钠溶液与醋酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com