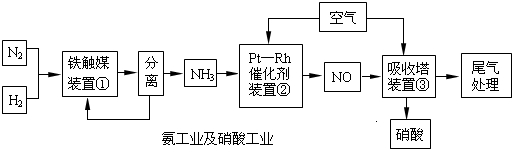
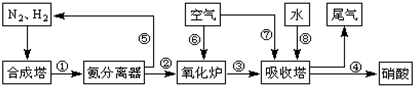
工业合成氨与制备硝酸一般可连续生产,流程如下:
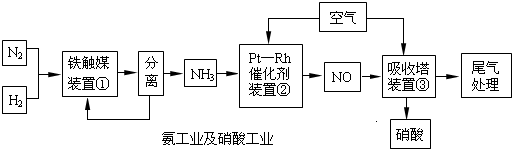
完成下列问题:
Ⅰ.合成氨
(1)写出装置①中发生反应的化学方程式:______.
(2)已知在一定的温度下进入装置①的氮、氢混合气体与从合成塔出来的混合气体压强之比为5:4,则氮的转化率为______.
Ⅱ.氨的接触氧化原理
(3)在900℃装置②中反应有:?
4NH
3(g)+5O
2(g)?4NO(g)+6H
2O(g);△H=-905.5kJ?mol
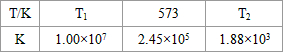
-1 K
1=1×10
53 (900℃)
4NH
3(g)+4O
2(g)?4N
2O(g)+6H
2O(g);△H=-1103kJ?mol
-1 K
2=1×10
61 (900℃)
4NH
3(g)+3O
2(g)?2N
2(g)+6H
2O(g);△H=-1267kJ?mol
-1 K
3=1×10
67 (900℃)
除了上列反应外,氨和一氧化氮相互作用:
4NH
3(g)+6NO(g)?5N
2(g)+6H
2O(g);△H=-1804kJ?mol
-1,还可能发生氨、一氧化氮的分解.
完成热化学方程式:2NO(g)?N
2(g)+O
2(g);△H=______.
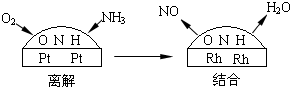
(4)铂-铑合金催化剂的催化机理为离解和结合两过程,如图所示:
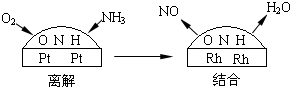
由于铂对NO和水分子的吸附力较小,有利于氮与氧原子结合,使得NO和水分子在铂表面脱附,进入气相中.若没有使用铂-铑合金催化剂,氨氧化结果将主要生成______.说明催化剂对反应有______.
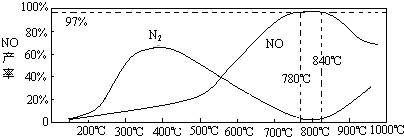
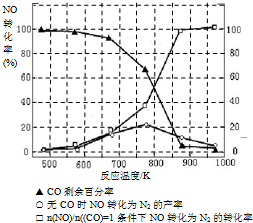
(5)温度对一氧化氮产率的影响
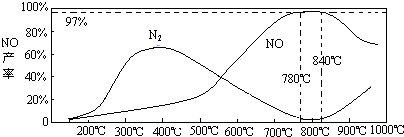
当温度大于900℃时,NO的产率下降的原因______(选填序号)
A.促进了一氧化氮的分解
B.促进了氨的分解
C.使氨和一氧化氮的反应平衡移动,生成更多N
2(6)硝酸工业的尾气常用Na
2CO
3溶液处理,尾气的NO、NO
2可全部被吸收,写出用Na
2CO
3溶液吸收的反应方程式______.






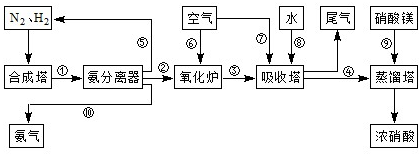
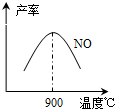 (3)NH3和O2在铂系催化剂作用下从145℃就开始反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905kJ?mol-1,不同温度下NO产率如右图所示.温度高于900℃时,NO产率下降的原因
(3)NH3和O2在铂系催化剂作用下从145℃就开始反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905kJ?mol-1,不同温度下NO产率如右图所示.温度高于900℃时,NO产率下降的原因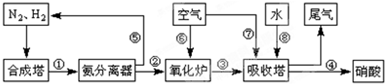
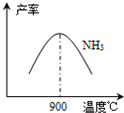 (3)N2和H2在铁作催化剂作用下从145℃就开始反应,不同温度下NH3产率如图所示.温度高于900℃时,NH3产率下降的原因
(3)N2和H2在铁作催化剂作用下从145℃就开始反应,不同温度下NH3产率如图所示.温度高于900℃时,NH3产率下降的原因