
 的说法正确的是( )
的说法正确的是( )| A. | 所有碳原子有可能都在同一平面上 | |
| B. | 最多只可能有9个碳原子在同一平面上 | |
| C. | 有5个碳原子可能在同一直线上 | |
| D. | 至少有6个碳原子在同一直线上 |
分析 碳碳三键为直线结构,苯环、碳碳双键为平面结合,甲基为四面体结构,以此来解答.
解答 解:A.碳碳三键为直线结构,苯环、碳碳双键为平面结合,且直接相连,则所有碳原子有可能都在同一平面上,故A正确;
B.由选项A可知,最多只可能有11个碳原子在同一平面上,故B错误;
C.碳碳三键及与苯环相连的C及对位C、双键上1个C位于同一直线上,即有5个碳原子可能在同一直线上,故C正确;
D.由选项C可知,有5个碳原子可能在同一直线上,故D错误;
故选AC.
点评 本题考查有机物的结构与性质,为高频考点,把握双键、三键及苯环结构为解答的关键,侧重分析与应用能力的考查,注意甲基为四面体结构,题目难度不大.


 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 10min内NaCl浓度变化表示的速率v(NaCl)=0.005 mol•L-1•min-1 | |
| B. | 若保持其他条件不变,在恒压下进行该反应,则平衡时NO2的转化率大于50% | |
| C. | 若升高温度,平衡逆向移动,则该反应的△H>0 | |
| D. | 若起始时向容器中充入0.2molNO2(g)、0.1molNO(g)和0.1molCl2(g)(固体物质足量),则反应将向正反应方向进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯乙烷与水互不相溶 | |
| B. | 氯乙烷中含有两种官能团 | |
| C. | 氯乙烷在一定条件下能发生消去反应 | |
| D. | 氯乙烷的结构只有一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 盐酸 | 矿泉水 | 硫酸 | 醋酸 | 干冰 |
| B | 氢氧化钡 | 蔗糖溶液 | 硫酸钡 | 溴水 | 二氧化硫 |
| C | 胆矾 | 石灰水 | 氧化铝 | 水 | 氯气 |
| D | 小苏打 | 氢氧化铁胶体 | 氯化银 | 一水合氨 | 酒精 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
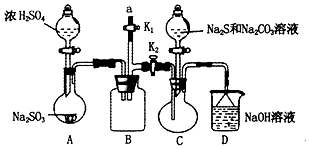 硫代硫酸钠(Na2S2O3)是重要的化工原料,易溶于水,在中性或碱性环境中稳定,在酸性条件下易分解,在空气中易被氧化.某化学兴趣小组通过如图装置(省略夹持装置)制备Na2S2O3.
硫代硫酸钠(Na2S2O3)是重要的化工原料,易溶于水,在中性或碱性环境中稳定,在酸性条件下易分解,在空气中易被氧化.某化学兴趣小组通过如图装置(省略夹持装置)制备Na2S2O3.| 实验序号 | 溶液pH | 亚硫酸钠与水的质量比 | 反应温度 | 硫粉质量 | 亚硫酸钠转化率 |
| 1 | 10 | 1.5:1 | 100℃ | 18 | 80.7% |
| 2 | 10 | 1.1:1 | 100℃ | 18 | 94.6% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
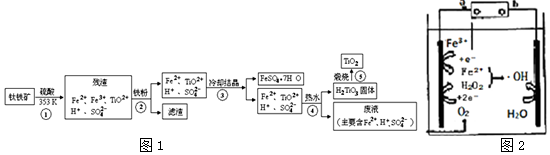
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
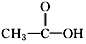 和
和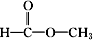 两种.为对其结构进行鉴定,物理方法可用红外光谱法或核磁共振氢谱法.
两种.为对其结构进行鉴定,物理方法可用红外光谱法或核磁共振氢谱法.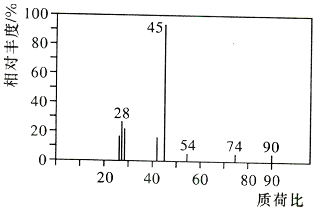
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该有机物属于烃 | B. | 该化合物的分子式一定是CH4O | ||
| C. | 无法确定该化合物是否含有氧元素 | D. | 该化合物中一定不含有氧元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com