
| 元素代号 | M | Q | A | D | R | E | T |
| 原子半径/nm | 0.037 | 0.160 | 0.077 | 0.075 | 0.089 | 0.102 | 0.074 |
| 主要化 合价 | +1 | +2 | +4、+2 | +5、-3 | +2 | +6、-2 | -2 |
| A. | Q、R的单质与稀盐酸反应的剧烈程度Q<R | |
| B. | T、Q形成的简单离子核外电子数相同 | |
| C. | 化合物AM4、DM3、M2T的稳定性逐渐减弱 | |
| D. | 化合物M2T2、ET2均具有漂白性,且漂白原理相同 |
分析 在短周期元素中,Q、R化合价为+2价,处于ⅡA族,原子半径Q>R,故Q为Mg,R为Be;E和T的化合价都有-2价,处于ⅥA族,E的最高价为+6价,T无正价,E为S元素,T为O元素;A有+4价,处于ⅣA族,D有+5、-3价,处于VA族,原子半径均小于S,故A为碳元素、D为N元素;M有+1价,处于IA族,原子半径小于氮,故M为H元素,结合元素周期律与元素化合物知识解答该题.
解答 解:在短周期元素中,Q、R化合价为+2价,处于ⅡA族,原子半径Q>R,故Q为Mg,R为Be;E和T的化合价都有-2价,处于ⅥA族,E的最高价为+6价,T无正价,E为S元素,T为O元素;A有+4价,处于ⅣA族,D有+5、-3价,处于VA族,原子半径均小于S,故A为碳元素、D为N元素;M有+1价,处于IA族,原子半径小于氮,故M为H元素.
A.金属性Mg>Be,则Mg与酸反应越剧烈,则相同条件下单质与稀盐酸反应速率为Q>R,故A错误;
B.O2-核外有10个电子,Mg2+核外有10个电子,二者核外电子数相同,故B正确;
C.非金属性C<N<O,故氢化物稳定性CH4、NH3、H2O的稳定性逐渐增强,故C错误;
D.化合物H2O2、SO2均具有漂白性,前者利用其强氧化性,后者与有色物质化合为不稳定无色物质,二者漂白原理不相同,故D错误,
故选:B.
点评 本题考查元素位置结构和性质的关系及应用,题目难度中等,正确把握元素化合价、原子半径与元素性质的关系是解答该题的关键,注意元素周期律的递变规律的应用.


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:选择题
| A. | ②④⑦⑧⑨⑩ | B. | ②④⑦⑨⑩ | C. | ③④⑦⑩ | D. | ④⑤⑦⑨⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 乙醇与钠反应,键①断裂 | |
| B. | 乙醇在Ag催化作用下与O2反应,键①③断裂 | |
| C. | 乙醇完全燃烧时,只有①②键断裂 | |
| D. | 乙醇、乙酸和浓硫酸共热制乙酸乙酯,键①断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑥⑦ | B. | ①④⑤ | C. | ①④⑥ | D. | ②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
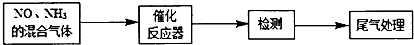
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯可作水果的催熟剂 | B. | SO2可用于杀菌消毒 | ||
| C. | 2H和3H可用于制造氢弹 | D. | 裂化汽油可用作萃取剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 要检验某溴乙烷中的溴元素,可以加入NaOH溶液共热,冷却后滴入AgNO3溶液,观察有无浅黄色沉淀生成 | |
| B. | 用乙醇制取乙烯时所用温度计的位置与石油分馏时所用温度计的位置不同 | |
| C. | 用氨水清洗试管壁附着的银镜 | |
| D. | 制取乙炔时药品是电石和饱和食盐水,仪器用启普发生器 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
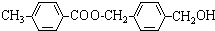 ,从A出发,可发生图示中的一系列反应.其中M属于高分子化合物,J和K互为同分异构体,N的产量可作为衡量一个国家石油化工发展水平的标志.
,从A出发,可发生图示中的一系列反应.其中M属于高分子化合物,J和K互为同分异构体,N的产量可作为衡量一个国家石油化工发展水平的标志.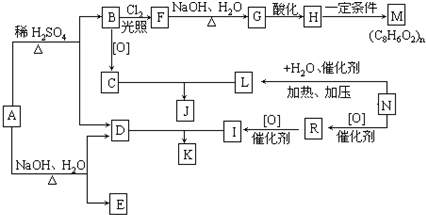
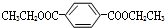 K
K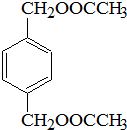
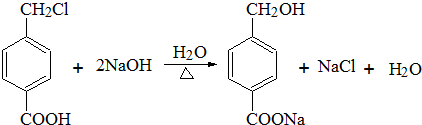 ;
;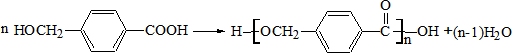 ;
;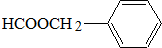 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com