
| A. | 铝 | B. | 铜 | C. | 锌 | D. | 银 |
分析 假设金属都为+2价,根据电子转移守恒计算金属物质的量,再计算平均相对原子质量,利用平均值法判断,注意金属不与酸反应,其相对原子质量视作无穷大,根据相对原子质量之比等于化合价之比计算Al为+2价的相对原子质量.
解答 解:2.24L氢气的物质的量为:$\frac{2.24L}{22.4L/mol}$=0.1mol,假设金属都为+2价,由电子转移守恒可知金属物质的量为0.1mol,则金属混合物的平均相对原子质量为$\frac{5}{0.1}$=50,Fe的相对原子质量为56,则另外金属的相对原子质量应小于50,且与盐酸反应生成氢气,
Cu、Ag与盐酸不反应,它们的相对原子质量视作无穷大,当Al的化合价为+2价时,其相对原子质量为$\frac{2}{3}$=18,Zn的相对原子质量为65,故选项中只有Al符合,
故选:A.
点评 本题考查混合物的计算,题目难度中等,本题利用平均值法解答,注意化合价与相对原子质量的转化.


科目:高中化学 来源: 题型:选择题
| A. | 定容时俯视观察液面 | |
| B. | 容量瓶中原有少量蒸馏水 | |
| C. | 溶解所用的烧杯、玻璃棒未洗涤 | |
| D. | 转移溶液时不慎将少量液体洒落在外 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
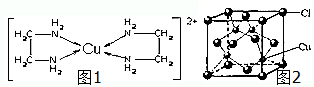 CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.已知:
CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.已知:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{(n-2m)}{V}mol•{L^{-1}}$ | B. | $\frac{(n-m)}{V}mol•{L^{-1}}$ | C. | $\frac{(2n-2m)}{V}mol•{L^{-1}}$ | D. | $\frac{(2n-4m)}{V}mol•{L^{-1}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | ②④⑤ | C. | ②③⑤ | D. | ②③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2S+2HCl=H2S↑+2NaCl | B. | FeSO4+H2S=FeS↓+H2SO4 | ||
| C. | CuSO4+H2S=CuS↓+H2SO4 | D. | ZnS+2HCl=H2S↑+ZnCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有两种原子构成的物质不一定属于化合物 | |
| B. | 仅含一种元素的物质一定为纯净物 | |
| C. | 既能和酸又能和碱发生反应的氧化物一定为两性氧化物 | |
| D. | 既含有金属元素又含有非金属元素的化合物一定为离子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com