
【题目】在一定温度下的定容容器中,当下列哪些物理量不再发生变化时,表明反应A(g)+2B(g)=C(g)+D(g)已达到平衡状态
①混合气体的压强②混合气体的密度③B的物质的量浓度④混合气体总物质的量⑤混合气体的平均相对分子质量⑥v(C)与v(D)的比值⑦混合气体总质量⑧混合气体总体积
A. ①②③④⑤⑥⑦⑧ B. ①③④⑤ C. ①②③④⑤⑦ D. ①③④⑤⑧
科目:高中化学 来源: 题型:
【题目】下列萃取与分液结合进行的操作(用CCl4为萃取剂从碘水中萃取碘)中错误的是
A.饱和碘水和CCl4加入分液漏斗中后,塞上上口部的塞子,用左手压住分液漏斗上口部,右手握住活塞部分,把分液漏斗倒转过来振荡
B.静置,分液漏斗中溶液分层,下层呈紫红色,上层几乎无色
C.打开分液漏斗的活塞,使全部下层液体沿承接液体的烧杯内壁慢慢流出
D.最后继续打开活塞用另一个烧杯承接上层液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是
A.标准状况下,22.4 L空气含有NA个单质分子
B.常温常压下,0.1 mol Na2CO3含有的Na+数目为0.2NA
C.标准状况下,22.4 L H2O含有的分子数为 NA
D.物质的量浓度为0.5 mol·L1的MgCl2溶液中,含有Cl个数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】689 K时,在1 L密闭容器中进行的反应:H2(g)+I2(g)![]() 2HI(g)达到平衡,图甲表示当起始物为1 mol·L-1 H2和1 mol·L-1 I2时,容器内各物质的浓度c的变化与时间t的关系示意图。
2HI(g)达到平衡,图甲表示当起始物为1 mol·L-1 H2和1 mol·L-1 I2时,容器内各物质的浓度c的变化与时间t的关系示意图。
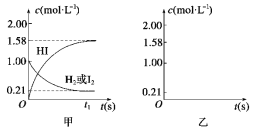
(1)请在图乙中画出当起始物为2 mol·L-1 HI时,容器中各物质的浓度变化与时间的关系示意图。
(2)由图中的事实说明化学平衡具有的特征是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与下列事实对应的化学用语不正确的是( )
A.用热的纯碱溶液可以清洗油污:CO32﹣+H2O?HCO3﹣+OH﹣
B.配制FeSO4溶液时加入适量的铁粉:Fe3++Fe═2Fe2+
C.向NH4HSO4溶液中加过量的NaOH溶液并加热:NH4++H++2OH﹣ ![]() NH3↑+2H2O
NH3↑+2H2O
D.铝片溶于较浓的NaOH溶液中,产生气体:2Al+2OH﹣+2H2O═2AlO2﹣+3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在200℃时,将a mol H2(g)和b mol I2(g)充入到体积为V L的密闭容器中,发生反应:I2(g)+H2(g)2HI(g)。
(1)反应刚开始时,由于c(H2)=______,c(I2)=______,而c(HI)=________,所以化学反应速率________最大而________最小(为零)(填“v正”或“v逆”)。
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为c(H2)________,c(I2)________,而c(HI)________,从而化学反应速率v正________,而v逆________(填“增大”、“减小”或“不变”)。
(3)当反应进行到v正与v逆________时,此可逆反应就达到了最大限度,若保持外界条件不变时,混合物中各组分的物质的量、物质的量浓度、质量分数、体积分数、反应物的转化率和生成物的产率及体系的总压强(或各组分的分压)都将________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二硫醇(HSCH2CH2SH)是一种难溶于水的精细化工产品,熔点﹣41℃,沸点 144℃,具有弱酸性.实验室以硫脲和1,2﹣二溴乙烷为原料制取乙二硫醇钠的合成路线如下: 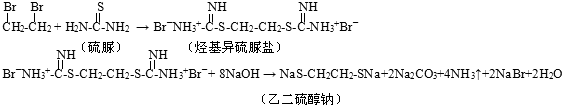
制备装置如图1所示(加热和夹持装置已略).
回答下 列问题:
(1)取适量硫脲于三口瓶中,加入乙醇,加热溶解,再加入1,2﹣二溴乙烷.一段时间后,有烃基异硫脲盐析出.冷凝管的作用 . 使用仪器a而不用普通分液漏斗的优点是 .
(2)过滤,得到烃基异硫脲盐晶体.从滤液中回收乙醇的操作是 . (填操作名称)
(3)仍使用图1的装置,将烃基异硫脲盐晶体和适量NaOH溶液加热1.5小时,冷却,再加入稀H2SO4即可得乙二硫醇. ①加入稀H2SO4生成乙二硫醇的化学方程式为 .
②从反应后的混合物中分离乙二硫醇的操作是 . (填操作名称)
③使用该装置有一个明显缺陷,改进的措施是 .
(4)理论上,制取9.4g乙二硫醇(M=94gmol﹣1)的同时可以制得NaBrg.
(5)NaBr和Na2SO4的溶解度随温度的变化如图2所示.简述从废液中提取Na2SO4的方法: .
(6)设计实验证明乙二硫醇中含有碳元素: . 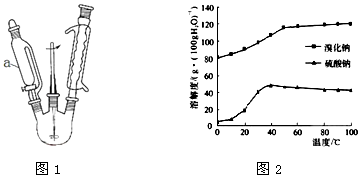
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在四种不同条件下测得反应2SO2+O2![]() 2SO3的反应速率如下表所示:
2SO3的反应速率如下表所示:
编号 | (1) | (2) | (3) | (4) |
反应速率[mol/(L·min)] | v(SO2) | v(O2) | v(SO3) | v(O2) |
0.4 | 0.25 | 0.5 | 0.3 |
其中反应速率最快的是( )
A.(1) B.(2) C.(3) D.(4)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com