
³£ĪĀŹ±£¬Ksp[Mg(OH)2] = 1.1”Į10£11£¬Ksp(AgCl) = 1.8”Į10£10£¬Ksp(Ag2CrO4) = 1.9”Į10£12£¬Ksp(CH3COOAg) = 2.3”Į10£3£¬ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ
A£®ÅØ¶Č¾łĪŖ0.2 mol”¤L£1µÄAgNO3ČÜŅŗŗĶCH3COONaČÜŅŗµČĢå»ż»ģŗĻŅ»¶Ø²śÉśCH3COOAg³Įµķ
B£®½«0.001 mol”¤L£1µÄAgNO3ČÜŅŗµĪČė0.001 mol”¤L£1µÄKClŗĶ0.001 mol”¤L£1µÄK2CrO4ČÜŅŗÖŠ£¬ĻČ²śÉśAg2CrO4³Įµķ
C£®c(Mg2+)ĪŖ0.11 mol”¤L£1µÄČÜŅŗÖŠŅŖ²śÉśMg(OH)2³Įµķ£¬ČÜŅŗµÄp£ČŅŖæŲÖĘŌŚ9ŅŌÉĻ
D£®ŌŚĘäĖūĢõ¼ž²»±äµÄĒéæöĻĀ£¬Ļņ±„ŗĶAgClĖ®ČÜŅŗÖŠ¼ÓČėNaClČÜŅŗ£¬Ksp(AgCl)²»±ä
B
”¾½āĪö”æŃ”ĻīAÖŠ»ģŗĻŗó£¬Ag£«ŗĶCH3COO£µÄÅØ¶Č¶¼ŹĒ0.1mol”¤L£1£¬¶žÕßµÄÅضČÖ®»żŹĒ0.01£¾2.3”Į10£3£¬ĖłŅŌŌ½¶ą²śÉś³Įµķ£¬AÕżČ·£»ŌŚĀČĄė×ÓÅضČŗĶCrO42£ÅØ¶Č¶¼ŹĒ0.001 mol”¤L£1Ź±£¬Éś³É³ĮµķŠčŅŖŅųĄė×ÓÅØ¶Č·Ö±šŹĒ1.8”Į10£7mol/LŗĶ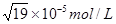 £¬ĖłŅŌŹ×ĻČÉś³ÉµÄŹĒĀČ»ÆŅų³Įµķ£¬B²»ÕżČ·£»øł¾ŻČܶȻż³£ŹżæÉÖŖ£¬µ±c(Mg2+)ĪŖ0.11 mol”¤L£1Ź±£¬ŅŖ²śÉśĒāŃõ»ÆĆ¾³ĮµķŠčŅŖOH£µÄÅØ¶ČŹĒ1.0”Į10£5mol/L£¬ĖłŅŌpHÖĮÉŁŅŖæŲÖĘŌŚ9ŅŌÉĻ£¬CÕżČ·£»ČܶȻż³£ŹżÖ»ÓėĪĀ¶ČÓŠ¹ŲĻµ£¬ĖłŅŌŃ”ĻīDÕżČ·£¬“š°øŃ”B”£
£¬ĖłŅŌŹ×ĻČÉś³ÉµÄŹĒĀČ»ÆŅų³Įµķ£¬B²»ÕżČ·£»øł¾ŻČܶȻż³£ŹżæÉÖŖ£¬µ±c(Mg2+)ĪŖ0.11 mol”¤L£1Ź±£¬ŅŖ²śÉśĒāŃõ»ÆĆ¾³ĮµķŠčŅŖOH£µÄÅØ¶ČŹĒ1.0”Į10£5mol/L£¬ĖłŅŌpHÖĮÉŁŅŖæŲÖĘŌŚ9ŅŌÉĻ£¬CÕżČ·£»ČܶȻż³£ŹżÖ»ÓėĪĀ¶ČÓŠ¹ŲĻµ£¬ĖłŅŌŃ”ĻīDÕżČ·£¬“š°øŃ”B”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
³£ĪĀŹ±£¬Ksp[Mg(OH)2] = 1.1”Į10£11£¬Ksp(AgCl) = 1.8”Į10£10£¬Ksp(Ag2CrO4) = 1.9”Į10£12 Ksp(CH3COOAg) = 2.3”Į10£3£¬ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ£Ø £©
A£®ÅØ¶Č¾łĪŖ0.2 mol”¤L£1µÄAgNO3ČÜŅŗŗĶCH3COONaČÜŅŗµČĢå»ż»ģŗĻŅ»¶Ø²śÉśCH3COOAg³Įµķ
B£®½«0.001 mol”¤L£1µÄAgNO3ČÜŅŗµĪČė0.001 mol”¤L£1µÄKClŗĶ0.001 mol”¤L£1µÄK2CrO4ČÜŅŗÖŠ£¬ĻČ²śÉśAg2CrO4³Įµķ
C£®c(Mg2+)ĪŖ0.11 mol”¤L£1µÄČÜŅŗÖŠŅŖ²śÉśMg(OH)2³Įµķ£¬ČÜŅŗµÄp£ČŅŖæŲÖĘŌŚ9ŅŌÉĻ
D£®ŌŚĘäĖūĢõ¼ž²»±äµÄĒéæöĻĀ£¬Ļņ±„ŗĶAgClĖ®ČÜŅŗÖŠ¼ÓČėNaClČÜŅŗ£¬Ksp(AgCl)²»±ä
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
³£ĪĀŹ±£¬Ksp[Mg(OH)2]= 1.1”Į10£11£¬Ksp(AgCl) = 1.8”Į10£10£¬Ksp(Ag2CrO4)= 1.9”Į10£12 Ksp(CH3COOAg)= 2.3”Į10£3£¬ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ£Ø £©
A£®ÅØ¶Č¾łĪŖ0.2 mol”¤L£1µÄAgNO3ČÜŅŗŗĶCH3COONaČÜŅŗµČĢå»ż»ģŗĻŅ»¶Ø²śÉśCH3COOAg³Įµķ
B£®½«0.001 mol”¤L£1µÄAgNO3ČÜŅŗµĪČė0.001 mol”¤L£1µÄKClŗĶ0.001 mol”¤L£1µÄK2CrO4ČÜŅŗÖŠ£¬ĻČ²śÉśAg2CrO4³Įµķ
C£®c(Mg2+)ĪŖ0.11 mol”¤L£1µÄČÜŅŗÖŠŅŖ²śÉśMg(OH)2³Įµķ£¬ČÜŅŗµÄp£ČŅŖæŲÖĘŌŚ9ŅŌÉĻ
D£®ŌŚĘäĖūĢõ¼ž²»±äµÄĒéæöĻĀ£¬Ļņ±„ŗĶAgClĖ®ČÜŅŗÖŠ¼ÓČėNaClČÜŅŗ£¬Ksp(AgCl)²»±ä
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2011-2012ѧğÕć½Ź”ŗ¼ÖŻŹŠøßČżÉĻѧʌµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ ĢāŠĶ£ŗŃ”ŌńĢā
³£ĪĀŹ±£¬Ksp[Mg(OH)2] = 1.1”Į10£11£¬Ksp(AgCl) = 1.8”Į10£10£¬
Ksp(Ag2CrO4) = 1.9”Į10£12 Ksp(CH3COOAg) = 2.3”Į10£3£¬ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ
A£®ÅØ¶Č¾łĪŖ0.2 mol”¤L£1µÄAgNO3ČÜŅŗŗĶCH3COONaČÜŅŗµČĢå»ż»ģŗĻŅ»¶Ø²śÉśCH3COOAg³Įµķ
B£®½«0.001 mol”¤L£1µÄAgNO3ČÜŅŗµĪČė0.001 mol”¤L£1µÄKClŗĶ0.001 mol”¤L£1µÄK2CrO4ČÜŅŗÖŠ£¬ĻČ²śÉśAg2CrO4³Įµķ
C£®c(Mg2+)ĪŖ0.11 mol”¤L£1µÄČÜŅŗÖŠŅŖ²śÉśMg(OH)2³Įµķ£¬ČÜŅŗµÄp£ČŅŖæŲÖĘŌŚ9ŅŌÉĻ
D£®ŌŚĘäĖūĢõ¼ž²»±äµÄĒéæöĻĀ£¬Ļņ±„ŗĶAgClĖ®ČÜŅŗÖŠ¼ÓČėNaClČÜŅŗ£¬Ksp(AgCl)²»±ä
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗÕć½Ź”Ī劣2009-2010ѧğ¶ČøßČżµŚŅ»“ĪĮŖ漣ػÆѧ£©ŹŌĢā ĢāŠĶ£ŗŃ”ŌńĢā
³£ĪĀŹ±£¬Ksp[Mg(OH)2] = 1.1”Į10£11£¬Ksp(AgCl) = 1.8”Į10£10£¬Ksp(Ag2CrO4) = 1.9”Į10£12 Ksp(CH3COOAg) = 2.3”Į10£3£¬ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ£Ø £©
A£®ÅØ¶Č¾łĪŖ0.2 mol”¤L£1µÄAgNO3ČÜŅŗŗĶCH3COONaČÜŅŗµČĢå»ż»ģŗĻŅ»¶Ø²śÉśCH3COOAg³Įµķ
B£®½«0.001 mol”¤L£1µÄAgNO3ČÜŅŗµĪČė0.001 mol”¤L£1µÄKClŗĶ0.001 mol”¤L£1µÄK2CrO4ČÜŅŗÖŠ£¬ĻČ²śÉśAg2CrO4³Įµķ
C£®c(Mg2+)ĪŖ0.11 mol”¤L£1µÄČÜŅŗÖŠŅŖ²śÉśMg(OH)2³Įµķ£¬ČÜŅŗµÄp£ČŅŖæŲÖĘŌŚ9ŅŌÉĻ
D£®ŌŚĘäĖūĢõ¼ž²»±äµÄĒéæöĻĀ£¬Ļņ±„ŗĶAgClĖ®ČÜŅŗÖŠ¼ÓČėNaClČÜŅŗ£¬Ksp(AgCl)²»±ä
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com