
| A�� | Fe��NO3��3��Һ�м��������HI��Һ��2Fe3++2I-�T2Fe2++I2 | |
| B�� | NH4HCO3��Һ�м��������NaOH��Һ�����ȣ�HCO3-+OH+$\frac{\underline{\;\;��\;\;}}{\;}$CO32-+H2O | |
| C�� | ϡ�����������Ag+2H++NO3-�TAg++NO��+H2O | |
| D�� | ����������Һ�м����������ữ�Ĺ���������Һ��2Fe2++2H++H2O2�T2Fe3++H2O |
���� A���⻯������������Ӻ���������Ӷ���ȫ��Ӧ��©�������������������ӵķ�Ӧ��
B��©���˰������������������ӵķ�Ӧ��
C������ת����Ŀ���غ㣻
D�������������ǿ�������ԣ��ܹ��������������ӣ�
��� �⣺A����������Һ�еμ�����HI��Һ�������Ӻ���������Ӷ����뷴Ӧ����ȷ�����ӷ���ʽΪ��Fe3++3NO3-+12H++10I-=Fe2++5I2+3NO��+6H2O����A����
B����NH4HCO3��Һ�мӹ�����NaOH��Һ�����ȣ����ӷ���ʽ��HCO3-+NH4++2OH-$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O+CO32-����B����
C������ϡ������ϴ����������Ӧ���Թܵ����ӷ�ӦΪ3Ag+4H++NO3-�T3Ag++NO��+2H2O����C����
D������������Һ�м����������ữ�Ĺ���������Һ��2Fe2++2H++H2O2�T2Fe3++H2O����D��ȷ��
��ѡ��D��
���� ���⿼�����ӷ�Ӧ����ʽ��д�������жϣ�Ϊ��Ƶ���㣬���շ����ķ�Ӧ�����ӷ�Ӧ����д����Ϊ���Ĺؼ���ע��ԭ�Ӹ�����������غ㣬��Ŀ�ѶȲ���


 �㽭��У��ʦ���ϵ�д�
�㽭��У��ʦ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���� | ���� | �����Լ� | ��Ӧ��������ӷ��� |
| A | �� | ���� | �ռ���Һ | ��Һ |
| B | �� | �� | ϡ���� | ���� |
| C | ���� | �Ȼ��� | ����ʳ��ˮ | ϴ�� |
| D | ���� | ��ϩ | ���� | ���������� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
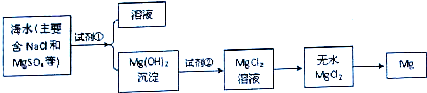
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
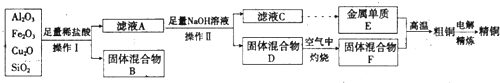
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1L1mol•L-1��NaClO��Һ�к���ClO-����ĿΪNA | |
| B�� | 88g���������д��ڵĹ��ۼ�����Ϊ14NA | |
| C�� | ����ʱ����2molH2SO4��Ũ����������ͭ��Ӧ��ת�Ƶĵ�����Ϊ2NA | |
| D�� | 1mol�ǻ������ĵ�����Ϊ10NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2 | B�� | PCl5 | C�� | NH3 | D�� | HClO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.2 mol | B�� | 0.25 mol | C�� | 0.3 mol | D�� | 0.35 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 | �� | �� | �� | �� | �� | �� | �� | �� |
| ԭ�Ӱ뾶��10-10m�� | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| �����ͻ��ϼ� | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com