
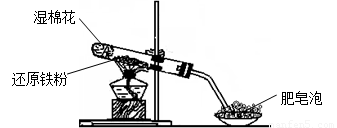
某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。
请回答下列问题:
(1)硬质试管中发生反应的化学方程式为____________________________________。
(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许固体物质于试管中,并向试管中加稀硫酸得溶液B;
②取少量溶液B于试管中,滴加几滴KSCN溶液,结果溶液未变红色,说明硬质试管中固体物质的成分有:____________________________。(填化学式)
(3)该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按图
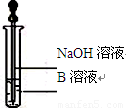
所示的操作,可观察到先生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关的反应的化学方程式:
① ;
② 。
(4)一段时间后,该同学发现(2)中未变红的溶液变成红色,说明Fe2+ 具有 性。由此可知,实验室中FeSO4溶液要临时配制并加少量铁粉的原因是 。(用离子方程式表示)
(1)3Fe+4H2O(g)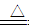 Fe3O4+4H2(2分) (2)Fe3O4和Fe(2分)
Fe3O4+4H2(2分) (2)Fe3O4和Fe(2分)
(3)FeSO4+2NaOH==Na2SO4+2Fe(OH) 2↓ (2分)
4Fe(OH) 2+ O2+2H2O==4Fe(OH) 3 (2分)
(4)还原(2分)、2Fe3++ Fe==3Fe2+ (2分)
【解析】
试题分析:(1)本题为铁与水蒸汽的反应实验,硬质试管中发生反应的化学方程式为:
3Fe+4H2O(g)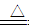 Fe3O4+4H2,(2)滴加几滴KSCN溶液,结果溶液未变红色,说明该溶液中并没有铁离子,说明铁离子被铁还原为亚铁离子,所以固体物质的成分为Fe3O4和Fe;(3)B溶液中含有亚铁离子,所以加入NaOH溶液,生产了白色的氢氧化亚铁沉淀,由于氢氧化亚铁不稳定,其在空气中能够被氧化为红褐色的氢氧化铁沉淀,所以相关的反应的化学方程式为:FeSO4+2NaOH==Na2SO4+2Fe(OH)
2↓、4Fe(OH) 2+ O2+2H2O==4Fe(OH)
3 ;(4)一段时间后,该同学发现(2)中未变红的溶液变成红色,说明有铁离子的生成,所以说明了亚铁离子具有还原性;故在实验室中FeSO4溶液要临时配制并加少量铁粉的原因是为了防止亚铁离子被氧化,其离子方程式为2Fe3++ Fe==3Fe2+ 。
Fe3O4+4H2,(2)滴加几滴KSCN溶液,结果溶液未变红色,说明该溶液中并没有铁离子,说明铁离子被铁还原为亚铁离子,所以固体物质的成分为Fe3O4和Fe;(3)B溶液中含有亚铁离子,所以加入NaOH溶液,生产了白色的氢氧化亚铁沉淀,由于氢氧化亚铁不稳定,其在空气中能够被氧化为红褐色的氢氧化铁沉淀,所以相关的反应的化学方程式为:FeSO4+2NaOH==Na2SO4+2Fe(OH)
2↓、4Fe(OH) 2+ O2+2H2O==4Fe(OH)
3 ;(4)一段时间后,该同学发现(2)中未变红的溶液变成红色,说明有铁离子的生成,所以说明了亚铁离子具有还原性;故在实验室中FeSO4溶液要临时配制并加少量铁粉的原因是为了防止亚铁离子被氧化,其离子方程式为2Fe3++ Fe==3Fe2+ 。
考点:铁及其化合物
点评:本题考查了铁及其化合物,该考查是高考考查的重点和热点,本题考查的基本上都是课本上的知识,本题难度适中。


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省济宁市泗水一中高一上学期期末模拟化学试卷(带解析) 题型:实验题
(17分)某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。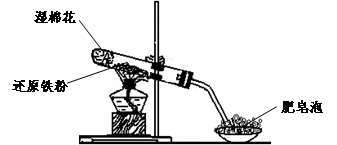
已知:①FeO + 2H+ = Fe2+ + H2O②Fe2O3 + 6H+ = 2Fe3+ +3 H2O ③Fe3O4 + 8H+ = Fe2+ +2Fe3+ +4 H2O
请回答下列问题:
(1)硬质试管中发生反应的化学方程式为 。
(2)该同学欲确定反应一段时间后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分是(只有一个选项符合题意) ,若溶液未变红色则说明硬质试管中固体物质的成分是(只有一个选项符合题意) 。
| A.一定有Fe3O4,可能有Fe | B.只有Fe(OH)3 | C.一定有Fe3O4和Fe |
| D.一定有Fe(OH)3,可能有Fe E.只有Fe3O4 |


查看答案和解析>>
科目:高中化学 来源:2011-2012学年四川省成都铁中高一下学期2月学业检测化学试卷 题型:实验题
(13分)某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。
请回答下列问题:
(1)硬质试管中发生反应的化学方程式为____________________________ 。
(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分一定有 ,可能有 ,若溶液未变红色则说明硬质试管中固体物质的成分是 。
(3)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是:
(用离子方程式表示)。
(4)该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出上述白色沉淀变成红褐色的化学方程式: 
(5)一段时间后,该同学发现(3)中未变红的溶液变成红色,
说明Fe2+ 具有 性。由此可知,实验室中含Fe2+的盐溶液现用现配制的原因是 ,并且配制含Fe2+的盐溶液时应加入少量 。
查看答案和解析>>
科目:高中化学 来源:2013学年江西省、铅山一中、弋阳一中高一第三次月考化学试卷(解析版) 题型:填空题
某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。

请回答下列问题:
(1)硬质试管中发生反应的化学方程式为____________________________ 。
(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分一定有 ,可能有 ,若溶液未变红色则说明硬质试管中固体物质的成分是 。
(3)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是:
(用离子方程式表示)。
(4)该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按右图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出上述白色沉淀变成红褐色的化学方程式: 。

(5)一段时间后,该同学发现(3)中未变红的溶液变成红色,说明Fe2+ 具有 性。由此可知,实验室中含Fe2+的盐溶液现用现配制的原因是 ,并且配制含Fe2+的盐溶液时应加入少量 。
查看答案和解析>>
科目:高中化学 来源:2014届四川省高一下学期2月学业检测化学试卷 题型:实验题
(13分)某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。
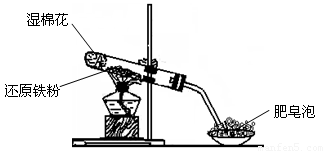
请回答下列问题:
(1)硬质试管中发生反应的化学方程式为____________________________ 。
(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分一定有 ,可能有 ,若溶液未变红色则说明硬质试管中固体物质的成分是 。
(3)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是:
(用离子方程式表示)。
(4)该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出上述白色沉淀变成红褐色的化学方程式:
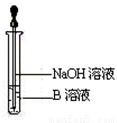
(5)一段时间后,该同学发现(3)中未变红的溶液变成 红色,
说明Fe2+ 具有 性。由此可知,实验室中含Fe2+的盐溶液现用现配制的原因是 ,并且配制含Fe2+的盐溶液时应加入少量 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com