
| A. | 石油的分馏和煤的干馏均属物理变化 | |
| B. | BaSO4在医学上用做钡餐,Ba2+对人体无毒 | |
| C. | 14C可用于文物的年代鉴定,14C与12C互为同位素 | |
| D. | 常温下铁与浓硫酸中不能反应,故通常用铁罐盛装浓硫酸 |
分析 A.石油的分馏是利用物质的沸点不同进行分离属物理变化,煤的干馏属于化学变化;
B.Ba2+被吸收后会对人体蛋白质产生变性;
C.质子数相同中子数不同的原子互称同位素;
D.常温下,铁和冷的浓硫酸反应生成一层致密的氧化物薄膜而发生钝化现象.
解答 解:A.石油的分馏属于物理变化,煤的干馏是指煤在隔绝空气的条件下加热,生成煤焦油、焦炭、焦炉煤气等物质属于化学变化,故A错误;
B.BaSO4难溶于水和酸,在医学上用做钡餐,Ba2+属于重金属离子能对人体蛋白质产生变性,对人体有毒,故B错误;
C.12C和14C质子数相同都为6,中子数分别为6、8不同,互为同位素,故C正确;
D.常温下,Fe和冷的浓硫酸反应生成一层致密的氧化物薄膜而阻止进一步被氧化,该现象为钝化现象,不是Fe和浓硫酸不反应,故D错误;
故选C.
点评 本题考查化学与生产、生活有关知识,掌握石油的分馏和煤的干馏、变性、同位素、钝化等知识是解答关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1000 mL | B. | 500 mL | C. | 100 mL | D. | 1500 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质和葡萄糖在一定条件下完全燃烧都只生成CO2和水 | |
| B. | 75%(体积分数)的乙醇溶液常用于医疗消毒 | |
| C. | 石油的分馏和煤的干馏均属于物理变化 | |
| D. | 乙烯和苯都能使溴水褪色,褪色的原因相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
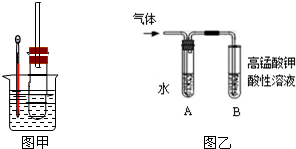 用如图实验装置(铁架台、酒精灯略) 验证溴乙烷的性质:
用如图实验装置(铁架台、酒精灯略) 验证溴乙烷的性质:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
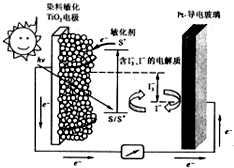 如图是一种染料敏化太阳能电池的示意图.电池的一个点极由有机光敏燃料(S)涂覆在TiO2纳米晶体表面制成,另一电极由导电玻璃镀铂构成,电池中发生的反应为:
如图是一种染料敏化太阳能电池的示意图.电池的一个点极由有机光敏燃料(S)涂覆在TiO2纳米晶体表面制成,另一电极由导电玻璃镀铂构成,电池中发生的反应为:| A. | 电池工作时,是将太阳能转化为电能 | |
| B. | 电池中镀铂导电玻璃为正极 | |
| C. | 电池工作时,I-离子在镀铂导电玻璃电极上放电 | |
| D. | 电池的电解质溶液中I-和I3-的浓度不会减少 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com