
| A. | 明矾净水:Al3++3H2O═Al(OH)3↓+3H+ | |
| B. | 硫酸镁与氢氧化钡溶液混合:SO${\;}_{4}^{2-}$+Ba2+═BaSO4↓ | |
| C. | 磷酸二氢钙与足量烧碱溶液反应:3Ca2++2H2PO${\;}_{4}^{-}$+4OH-═Ca3(PO4)2↓+4H2O | |
| D. | 氨水中通入过量的二氧化硫气体:NH3•H2O+SO2═NH${\;}_{4}^{+}$+HSO${\;}_{3}^{-}$ |
分析 A.生成胶体,不是沉淀;
B.漏写生成氢氧化镁的离子反应;
C.不符合离子的配比;
D.反应生成亚硫酸氢铵.
解答 解:A.明矾净水的离子反应为Al3++3H2O═Al(OH)3(胶体)+3H+,故A错误;
B.硫酸镁与氢氧化钡溶液混合的离子反应为2OH-+Mg2++SO42-+Ba2+═BaSO4↓+Mg(OH)2↓,故B错误;
C.磷酸二氢钙与足量烧碱溶液反应的离子反应为3Ca2++6H2PO4-+12OH-═Ca3(PO4)2↓+6H2O+4PO43-,故C错误;
D.氨水中通入过量的二氧化硫气体的离子反应为NH3•H2O+SO2═HSO3-+NH4+,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 将CO中毒者移至通风处抢救 | |
| B. | 误食硫酸铜溶液,可服用氢氧化钠溶液解毒 | |
| C. | 浓H2SO4溅到皮肤上,立即用碳酸钠稀溶液洗涤 | |
| D. | 氢氧化钠浓溶液溅入眼中,应立即用大量水冲洗,再用稀盐酸冲洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
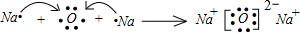 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其它条件不变,加入催化剂,△H变大 | |
| B. | 及时除去二氧化碳,能使NO完全转化 | |
| C. | 充入氦气使体系压强增大,可提高反应物的转化率 | |
| D. | 若升高温度,该反应的平衡常数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③④ | C. | ①③ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠在空气中燃烧可生成多种氧化物,23g钠充分燃烧时转移电子数为1NA | |
| B. | 标准状况下,1.12L氦气所含原子数为0.1NA | |
| C. | 17gNH3所含电子数目为NA | |
| D. | 22.4LHCl溶于水,溶液中H+数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:
如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com