

| A.该硫酸具有强烈的腐蚀性,应放于危险化学用品柜中妥善保管 |
| B.取10 mL该硫酸于烧杯中,再加18.4 mL的水,可配得49%的硫酸 |
| C.配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL |
| D.该硫酸与等质量的水混合所得溶液的物质的量浓度小于9.2 mol/L |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.25 ℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA |
| B.0.1 mol·L-1的NaHSO4溶液中,阳离子的数目之和为0.2NA |
| C.0.1 mol Zn与含0.1 mol HCl的盐酸充分反应,转移电子数目为0.2NA |
| D.标准状况下,18 g H2O所含的氧原子数目为NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温常压下,2.24 L CH4中含有0.4NA个共价键 |
| B.100 mL l mol·L-1 Na[Al(OH)4]溶液中含有0.1以个[Al(OH)4]- |
| C.常温条件下,5.6gFe与足量稀HNO3反应,转移0.2NA个电子 |
| D.标准状况下,1.12 L 1H2和0.2g2H2均含有0.1NA个质子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X一定只由CO组成 |
| B.X一定只由H2和CO2组成 |
| C.X可能由0.1 g H2和4.4 g CO2组成 |
| D.X可能由0.1 g H2、1.4 g CO、2.2 g CO2组成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.9.2 g NO2气体中含有分子数目为0.2NA |
| B.标准状况下,2.24 L SO3中含有氧原子数目为0.3NA |
C.2 g 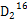 O中含中子、质子、电子数目均为NA O中含中子、质子、电子数目均为NA |
| D.标准状况下2.24 L Cl2通入足量水中或NaOH溶液中,转移电子数目均为0.1NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.6.0 mol·L-1 | B.3.0 mol·L-1 | C.9.0 mol·L-1 | D.4.5 mol·L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com