
分析 原电池的总反应为:2Fe3++Cu═2Fe2++Cu2+,Cu作负极,失电子发生氧化反应,正极材料是不如Cu活泼的金属或石墨电极,Fe3+在正极上得电子发生还原反应,据负极的电极反应式计算有1.28gCu反应时,转移电子的数目.
解答 解:(1)原电池的总反应为:2Fe3++Cu═2Fe2++Cu2+,Cu作负极,电极反应式为:Cu-2e-=Cu2+,故答案为:Cu;Cu-2e-=Cu2+;
(2)正极材料是不如Cu活泼的金属或石墨电极,Fe3+在正极上得电子发生还原反应,电极反应式为:2Fe3++2e-=2Fe2+;
故答案为:不如Cu活泼的金属或石墨电极;2Fe3++2e-=2Fe2+;
(3)Cu-2e-=Cu2+;
64g 2mol
1.28g n
n=$\frac{1.28g×2mol}{64g}$=0.04mol,转移电子个数为0.04NA,故答案为:0.04NA.
点评 本题考查了据氧化还原反应方程式设计原电池以及据电极反应式的计算,题目难度不大.


科目:高中化学 来源: 题型:多选题
| A. | 含氧酸的酸性:H3ZO4>H2YO4>HXO4 | |
| B. | 非金属性:X>Y>Z | |
| C. | 气态氢化物的稳定性按X、Y、Z顺序由弱到强 | |
| D. | 元素的负化合价的绝对值按X、Y、Z顺序由小到大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验序号 | (1) | (2) | (3) |
| 取用盐酸的体积/mL | 25 | 25 | 25 |
| 取用混合物的质量/g | 1.32 | 1.54 | 2.20 |
| 生成气体的体积(标准状况)/mL | 336 | 392 | 448 |
| A. | 1.2 | B. | 1.4 | C. | 1.6 | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ④⑤ | C. | ④ | D. | ⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
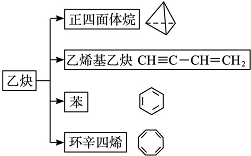
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色. |
| ②在盛有冷水的烧杯中滴入几滴酚酞溶液,再将一小块金属钠放入其中 | B.有气体产生,溶液变成浅红色 |
| ③将镁条投入稀盐酸中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将铝条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体. |
| ⑤向A1Cl3溶液中滴加NaOH溶液至过量 | E.生成白色胶状沉淀,继而沉淀消失 |
| 实验内容 | ① | ② | ③ | ④ | ⑤ |
| 实验现象(填A~F) | B |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com