
对于化学反应限度的叙述,错误的是( )
A.任何可逆反应都有一定的限度
B.化学反应达到限度时,正、逆反应速率相等
C.化学反应的限度与时间的长短无关
D.化学反应的限度是不可改变的
科目:高中化学 来源: 题型:
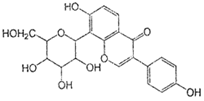
葛根素具有降血压等作用,其结构简式如下图,下列有关说法正确的是( )
A.该物质在一定条件下能发生消去反应、加成反应、取代反应
B.葛根素的分子式为C21H22O9
C.该物质一个分子中含有5个手性碳原子
D.一定条件下1 mol 该物质与H2反应最多能消耗7 mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中含有较大量的Cl-、CO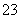 、OH-3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次沉淀出来,下列实验操作顺序正确的是( )
、OH-3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次沉淀出来,下列实验操作顺序正确的是( )
①滴加Mg(NO3)2溶液 ②过滤 ③滴加AgNO3溶液
④滴加Ba(NO3)2溶液
A.①②④②③ B.④②①②③
C.①②③②④ D.④②③②①
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B在D中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A在F中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)A在周期表中的位置是________,写出一种工业制备单质F的离子方程式____________________________________________________________________。
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为________,其水溶液与F单质反应的化学方程式为____________________________;在产物中加入少量KI,反应后加入CCl4并振荡,有机层显________色。
(3)由这些元素组成的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1:1 |
| c | 化学组成为BDF2 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
a的化学式为________;b的化学式为________;c的电子式为________;d的晶体类型是________。
(4)由A和B、D元素组成的两种二元化合物形成一类新能源物质。一种化合物分子通过________键构成具有空腔的固体;另一种化合物(沼气的主要成分)分子进入该空腔,其分子的空间结构为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有如下仪器,仪器中已注入溶液,回答下列问题。
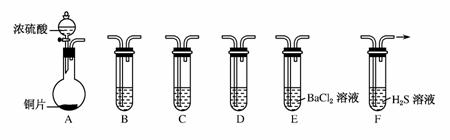
(1)加热装置A,写出铜与浓硫酸反应的化学方 程式_______________________________,烧瓶中的实验现象为________。
程式_______________________________,烧瓶中的实验现象为________。
(2)验证碳、硅非金属性的相对强弱(已知酸性:H2SO3>H2CO3),若选择仪器A、B、C、D并相连接,则B、C、D中所选择的试剂为B________、C________、D________。能说明碳的非金属性比硅强的实验现象是______________________。
(3)验证SO2的氧化性、还原性。若选择A、E、F仪器,并按A、E、F顺序连接。
①则证明SO2有氧化性的实验现象是______________________,反应方程式为______________________________。
②若证明SO2具有还 原性,在E中采取的实验操作为________,其实验现象为________,反应原理为____________________(用离子方程式表示)。
原性,在E中采取的实验操作为________,其实验现象为________,反应原理为____________________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
对处于平衡状态的反应2A(g)+B(g) 2C(g) △H<0,下
2C(g) △H<0,下
列叙述正确的是
A.增大A浓度的瞬间,V正 增大,V逆不变 B.升高温度,V正 减小,V逆增大
C.增大压强. V正 增大,V逆 减小 D.加入催化剂,V正、V逆 都增大
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下的某容积可变的密闭容器中,建立下列化学平衡:C(s)+H2O(g)CO(g)+H2(g)不能确
定上述可逆反应在一定条件下已达到化学平衡状态的是 ( )
A.体系的压强不再发生变化
B.v正(CO)=v逆(H2O)
C.生成n mol CO的同时生成n mol H2
D.1 mol H—H键断裂的同时断裂2 mol H—O键
查看答案和解析>>
科目:高中化学 来源: 题型:
镍具有优良的物理和化学特性,是许多领域尤其是高技术产业的重要原料。羰基法提纯粗镍涉及的两步反应依次为:
(1)Ni(S)+4CO(g) 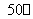 Ni(CO)4(g)+Q
Ni(CO)4(g)+Q
(2)Ni(CO)4(g)  Ni(S)+4CO(g)
Ni(S)+4CO(g)
完成下列填空:
(1)在温度不变的情况下,要提高反应(1)中Ni(CO4)的产率,可采取的措施有 、 。
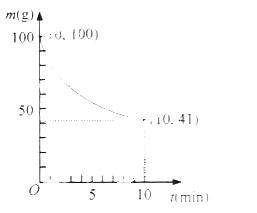
(2)已知在一定条件下的2L密闭容器中制备Ni(CO)4,粗镍(纯度98.5%,所含杂质不与CO反应)剩余质量和反应时间的关系如右图所示。Ni(CO)4在0~10min的平均反应速率为 。
(3)若反应(2)达到平衡后,保持其他条件不变,降低温度,重新达到平衡时 。
a.平衡常数K增大 b.CO的浓度减小
c.Ni的质量减小 d.v逆【Ni(CO)4】增大
(4)简述羰基法提纯粗镍的操作过程。
查看答案和解析>>
科目:高中化学 来源: 题型:
向一容积为1L 的密闭容器中加入一定量的X、Y,
发生化学反应aX(g)+2Y(s)  bZ(g) △H<0。下图是容器中X、Z的物质的量浓度随时间变化的曲线。
bZ(g) △H<0。下图是容器中X、Z的物质的量浓度随时间变化的曲线。
根据以上信息判断,下列说法中正确的是
A.用X表示0~ 10min内该反应的平均速率为v(X)=0.045mol/(L·min)
10min内该反应的平均速率为v(X)=0.045mol/(L·min)
B.化学方程式中a:b= 1:3,
C.推测在第7min时曲线变化的原因可能是增加X的浓度
D.推测该反应处于化学平衡状态的时间是10min--13min及第20min 后
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com