
【题目】汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3→K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75mol,则下列判断正确的是( )
A. 生成42.0LN2(标准状况)
B. 有0.250molKNO3被氧化
C. 转移电子的物质的量为2.25mol
D. 被氧化的N原子的物质的量为3.75mol
【答案】D
【解析】
根据反应方程式可知,每当生成16molN2,则氧化产物比还原产物多14mol,转移电子的物质的量为10mol,被氧化的N原子的物质的量为30mol,有2molKNO3被还原,现氧化产物比还原产物多1.75mol,则生成2molN2,转移电子的物质的量为1.25mol,被氧化的N原子的物质的量为3.75mol,据此答题。
10NaN3+2KNO3=K2O+5Na2O+16N2↑中N元素化合价由1/3、+5价变为0价,所以NaN3是还原剂、KNO3是氧化剂,N2既是氧化产物又是还原剂,根据反应方程式可以知道,每当生成16molN2,则氧化产物比还原产物多14mol,转移电子的物质的量为10mol,被氧化的N原子的物质的量为30mol,有2mol KNO3被还原,现氧化产物比还原产物多1.75mol,则生成2molN2,转移电子的物质的量为1.25mol,被氧化的N原子的物质的量为3.75mol。
A.生成2molN2,在标准状况下的体积为2mol×22.4L/mol=44.8L,故A错误;
B.由反应可以知道,NaN3发生氧化反应,KNO3发生还原反应,被还原的硝酸钾的物质的量为2mol×![]() =0.25mol,故B错误;
=0.25mol,故B错误;
C.结合方程式可知,参加反应KNO3的物质的量=2mol×2/16=0.25mol,中N元素化合价由+5价降低为0价,故转移电子为0.25mol×5=1.25mol,故C错误;
D.转移10mol电子被氧化的N原子为30mol,则转移1.25mol电子被氧化的N原子的物质的量为![]() =3.75mol,故D正确。
=3.75mol,故D正确。
故选D。


科目:高中化学 来源: 题型:
【题目】模拟工业上离子交换膜法制烧碱的方法,电解硫酸钾溶液可制备氢气、氧气、硫酸和氢氧化钾,装置如图所示。下列说法不正确的是( )
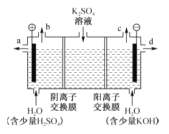
A. 通电开始后,阴极附近溶液pH增大
B. 制得的氢氧化钾溶液从出口d流出
C. 电解槽的阳极反应式为2H2O﹣4e-=4H++O2↑
D. 通过阴离子交换膜的离子数等于通过阳离子交换膜的离子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在元素周期表中的前四周期,两两相邻的5种元素如图所示,若B元素的核电荷数为a。下列说法正确的是( )

A. B、D的原子序数之差可能为2
B. E、B的原子序数之差可能是8、18或32
C. 5种元素的核电荷总数之和可能为5a+10
D. A、E的原子序数之差可能是7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为___________(写离子符号);若所得溶液c(HCO3)∶c(CO32)=2∶1,溶液pH=___________。(室温下,H2CO3的K1=4×107;K2=5×1011)
(2)CO2与CH4经催化重整,制得合成气:CH4(g)+ CO2(g) ![]() 2CO (g)+ 2H2(g)
2CO (g)+ 2H2(g)
已知上述反应中相关的化学键键能数据如下:
化学键 | C—H | C=O | H—H | C |
键能/kJ·mol1 | 413 | 745 | 436 | 1075 |
则该反应的ΔH=______。分别在VL恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1 mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是____(填“A” 或“B ”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D 四种短周期元素,A 与B 可形成离子化合物BA,BA 中阴阳离子的核外电子排布相同;B 原子最外层只有-个电子;C 元素有三种不同的核素C1、C2、C3,且三种核素的质量数之比为1:2:3;D 原子的质子数是A、B、C 三种原子质子数之和的![]() 。
。
回答下列问题:
(1)写出各元素的元素符号:A____,B____,C____,D____。
(2)写出C1、C2、C3三种核素的原子符号:C1____,C2_____,C3______。
(3)C、D 两种元素形成的微粒X 与化合物BA 中的阳离子所含的质子数和电子数分别相等,则X 的化学式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( )
①Fe![]() Fe2O3
Fe2O3![]() Fe2(SO4)3
Fe2(SO4)3
②SiO2![]() Na2SiO3
Na2SiO3![]() H2SiO3
H2SiO3
③AlCl3![]() Al
Al![]() NaAlO2
NaAlO2
④Na![]() Na2O
Na2O![]() NaOH
NaOH
⑤SO2![]() H2SO3
H2SO3![]() H2SO4
H2SO4
⑥饱和NaCl(ag)![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
A. ①②⑤B. ②③⑥C. ②⑤⑥D. ①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法错误的是
A. 标准状况下,30.8gCCl4中所含的原子数为NA
B. 100g46%乙醇溶液中含有的H-O键的数目为NA
C. 1molNa2O2与足量的CO2充分反应,转移的电子数为NA
D. n(H2SO3)+n(HSO3-)=1mol的NaHSO3溶液中,含有Na+的数目大于NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,离子方程式书写正确的是( )
A.向NaHCO3溶液中加入NaOH溶液:HCO3-+OH-=CO2↑+H2O
B.0.1mol/LNH4Al(SO4)2溶液与0.2mol/LBa(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH- =2BaSO4↓+AlO2-+2H2O
C.用醋酸除水垢:CaCO3+2H+=Ca2++H2O+CO2↑
D.硫酸溶液中滴加足量氢氧化钡溶液:2H++SO42-+Ba2++2OH-=2H2O+BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏伽德罗常数的值,下列说法不正确的是( )
A.常温常压下,14g有N2与CO组成的混合气体含有的原子数目为NA个
B.0.5molO3与11.2LO2所含的分子数一定相等
C.10gCaCO3和KHCO3的固体混合物含有0.1NA个阳离子
D.用16.25gFeCl3制备Fe(OH)3胶体,Fe(OH)3胶体粒子数小于0.1NA个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com