
| A. | 11种 | B. | 10种 | C. | 9种 | D. | 8种 |
分析 采取分类讨论书写法,当两个Br取代甲基上的H时、当有一个溴取代甲基上的H,另外一个溴取代苯环上的H时、当2个溴都取代苯环上的H时分别有多少中结构,注意不能重复书写,以此解答该题.
解答 解:甲苯中,①当两个Br取代甲基上的H时有1种结构;
②当有一个溴取代甲基上的H,另外一个溴取代苯环上的H,苯环上可以有邻、间、对3种位置,故二溴代物有3种结构;
③当2个溴都取代苯环上的H时,采用定一议二的方法,当其中一个溴在甲基的邻位时,另外一个溴还有4种位置,故此二溴代物有4种结构;当其中一个溴在甲基的间位时,另一个溴有2种位置,故二溴代物有2种结构,
综上所述,二溴代物的结构有1+3+4+2=10种,
故选B.
点评 本题考查了同分异构体的书写,为高频考点,侧重考查学生的分析能力,中等难度,解题关键要搞清取代基的异构体及等效H原子判断.


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:推断题
 .B的离子结构示意图:
.B的离子结构示意图: .D在周期表的位置:第3周期第ⅦA.写出C的原子符号2412Mg.
.D在周期表的位置:第3周期第ⅦA.写出C的原子符号2412Mg. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
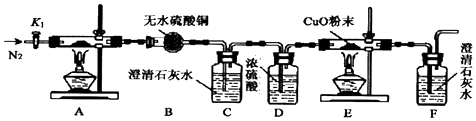
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/S | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/(10-4mol/L) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO)/(10-3mol/L) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
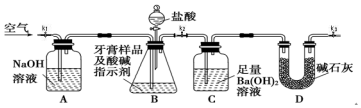
| 实验步骤 | 预期现象与结论 |
| 取适量牙膏样品于试管中,加入足量的NaOH溶液,过滤,向滤液中滴加盐酸. | 滤液中先出现白色沉淀,随后沉淀溶解,说明该牙膏摩擦剂中含氢氧化铝. |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| Cl2的体积 (标准状况下)/L | 2.8 | 5.6 | 11.2 |
| n(A-)/mol | 1.25 | 1.5 | 2 |
| n(B-)/mol | 1.5 | 1.4 | 0.9 |
| n(C-)/mol | a | 0 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 时间/min | 0 | 10 | 20 | 40 | 50 | |
| T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | … | 0.15 |
| A. | T1时0~10 min NO2的平均反应速率为0.15 mol•L-1•min-1 | |
| B. | T2时CH4的平衡转化率为70.0% | |
| C. | 保持其他条件不变,T1时向平衡体系中再充入0.30 mol CH4和0.80 mol H2O(g),平衡向正反应方向移动 | |
| D. | 保持其他条件不变,T1时向平衡体系中再充入0.50 mol CH4和1.20 mol NO2,与原平衡相比,达新平衡时N2的浓度增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com