
����Ŀ���±���Ԫ�����ڱ���һ���֣�����Ա������б��Ϊ�١����Ԫ�ػش��������⡣
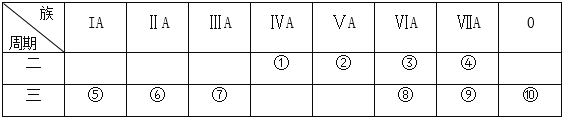
��1���ǽ�������ǿ��Ԫ����______(��Ԫ�ط��ţ���ͬ)���γɻ�������������Ԫ����_____������õ�Ԫ����___________��
��2����������Ԫ�س�����ԭ�Ӱ뾶��С����______(��Ԫ�ط���)����ЩԪ�ص�����������Ӧˮ�����м�����ǿ����__________(�ѧʽ����ͬ)���������Ե���____________������������Ӧˮ������������ǿ����__________��
��3���ޢߢ��γɵļ����ӵ���С�����˳���� ______________�������ӷ��Żش����⣩��
������Ӧ���⻯��Ƚ��ȶ�����_________���ѧʽ����
��4���ݺ͢ۿ����γ����ֻ�������п�����������߹����������ʵĵ���ʽΪ_________��������ѧ��������Ϊ _______________��
��5��������γɵĻ�����Ľṹʽ __________���õ���ʽ��ʾ ��������γɻ�������γɹ��� _________________________��
���𰸡� F C Ar Cl NaOH Al(OH)3 HClO4 Al3+<Mg2+<Cl- HCl ![]() ���Ӽ����Ǽ��Լ�
���Ӽ����Ǽ��Լ� ![]()
![]()
������������Ԫ�������ڱ��е�λ��֪���١����Ԫ�طֱ���C��N��O��F��Na��Mg��Al��S��Cl��ArԪ�ء�
(1)�ǽ�������ǿ��Ԫ��λ�����ڱ����Ͻǣ���ϡ��������⣬ΪFԪ�أ��γɻ�������������Ԫ����CԪ�أ�����õ�Ԫ���Ƕ���Ԫ�أ�ΪAr���ʴ�Ϊ��F��C��Ar��
(2)ͬһ����Ԫ�أ�ԭ�Ӱ뾶����ԭ�������������С�����Ե�������ԭ�Ӱ뾶��С��Ԫ����ClԪ��(ϡ���������)��Ԫ�صĽ�����Խǿ��������������ˮ�������Խǿ�����Ե������ڼ�����ǿ����NaOH�������Ե�����������������������ѧʽΪAl(OH)3��Ԫ�صķǽ�����Խǿ��������������ˮ��������Խǿ������������Ӧˮ������������ǿ����HClO4���ʴ�Ϊ��Cl��NaOH��Al(OH)3��HClO4��
(3)һ����ԣ����ӵĵ��Ӳ���Խ�࣬���Ӱ뾶Խ���Ӳ�����ͬʱ���˵����Խ�����Ӱ뾶ԽС���ޢߢ��γɵļ����ӵ���С�����˳��ΪAl3+<Mg2+<Cl-��Ԫ�صķǽ�����Խǿ���⻯��Խ�ȶ���������Ӧ���⻯��Ƚ��ȶ�����HCl���ʴ�Ϊ��Al3+<Mg2+<Cl-��HCl��
(4)�ݺ͢ۿ����γ����ֻ�����Ϊ�����ƺ������ƣ����п�����������߹�����������Ϊ�������ƣ�����ʽΪ![]() ��������ѧ��������Ϊ���Ӽ����Ǽ��Լ����ʴ�Ϊ��
��������ѧ��������Ϊ���Ӽ����Ǽ��Լ����ʴ�Ϊ��![]() �����Ӽ����Ǽ��Լ���
�����Ӽ����Ǽ��Լ���
(5)CS2�Ľṹ�������̼���ƣ��ṹʽΪ![]() ���Ȼ�þ�������ӻ�����õ���ʽ��ʾ�Ȼ�þ���γɹ���Ϊ
���Ȼ�þ�������ӻ�����õ���ʽ��ʾ�Ȼ�þ���γɹ���Ϊ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��![]() ��
��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��̷�����ѧ�仯����
A���������� B����ˮɹ�� C����ʳ��� D����ѩ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���ܴﵽԤ��Ŀ�ĵ���
A. ����ˮ�����������Ƿ��в�����֬����
B. ��ȥ���л��еı��ӣ�����Ũ��ˮ������
C. ��ȥ�Ҵ��л��е�ˮ����������ƣ�����
D. ���������л�����ϩ, ͨ�����Ը��������Һ��ϴ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(CeO2)��һ����Ҫ��ϡ�������ƽ�������ʾ�����������в��������ķϲ�����ĩ����SiO2��Fe2O3��CeO2��FeO�����ʣ���ij�������Դ˷�ĩΪԭ�ϣ�������¹������̶���Դ���л��գ��õ�������CeO2��������茶��塣
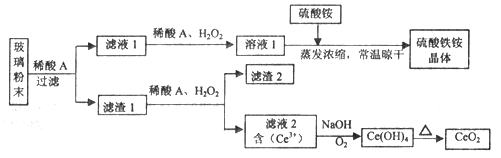
��֪��CeO2������ϡ���ᣬҲ������NaOH��Һ��
(1)ϡ��A�ķ���ʽ��_____________________��
(2)��Һ1�м���H2O2��Һ��Ŀ����__________________��
(3)���ʵ��֤����Һ1�к���Fe2+_____________________��
(4)��֪Fe2+��Һ���Ժ�������ˮ��FeO(OH)��Ӧ����Fe3O4,��д�÷�Ӧ�����ӷ���ʽ____________��
(5)����Һ2����Ce(OH)4�����ӷ���ʽ__________________��
(6)������茶���[Fe2(SO4)3��2(NH4)2SO4��3H2O]�㷺����ˮ�ľ���������������ȥ�����Է�ˮ�е�������ʱЧ�ʽ�������ԭ����___________________��
(7)ȡ���������еõ���Ce(OH)4��Ʒ0.531 g���������ܽ����Ũ��Ϊ0.l000mol��L-1FeSO 4����Һ�ζ����յ�ʱ���汻��ԭΪCe3+ )������25.00 mL����Һ���ò�Ʒ��Ce(OH)4�����÷���Ϊ_______(���������λ��Ч����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������̬�ĵ���һϵ��ת�����Եõ����ᣬ����ͼ��ʾ��
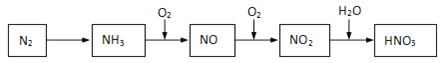
(1)NH3��O2�ڴ��������·�Ӧ���仯ѧ����ʽ��______________��
(2)NO2��HNO3��Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ________________��
(3)2NO(g)+O2(g) ![]() 2NO2(g)�������������Ҫ��Ӧ֮һ����800��ʱ�����ݻ�Ϊ1L���ܱ������г���0.010molNO��0.005molO2����Ӧ������NO��Ũ����ʱ��仯����ͼ��ʾ��
2NO2(g)�������������Ҫ��Ӧ֮һ����800��ʱ�����ݻ�Ϊ1L���ܱ������г���0.010molNO��0.005molO2����Ӧ������NO��Ũ����ʱ��仯����ͼ��ʾ��

��2min�ڣ�v(O2)=________mol/(L��min)
��800��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ__________��
���жϸ÷�Ӧ�ﵽƽ��������ǣ�д��2�����ɣ�____________��
����֪����.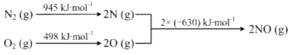
��.N2(g)+2O2(g)=2NO2(g) ��H=+68kJ��mol-1��д��NO����NO2�Ȼ�ѧ����ʽ_____________���¶ȶ���NO����NO2ƽ��ת���ʵ�Ӱ���ǣ�___________________��
(4)��ⷨ����������������������Ի������ᡣʵ����ģ���ⷨ����NO��װ����ͼ��ʾ����Ϊʯī�缫������д���缫������NOת��Ϊ����ĵ缫��Ӧʽ��______________��
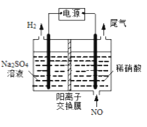
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NaHS��Һ�м���һ������CuSO4��Һ�������ķ�Ӧ�����ӷ���ʽ����Ϊ�� ��
A.S2��+Cu2+��CuS��
B.2HS��+Cu2+��CuS��+2H++S2��
C.HS��+Cu2+��CuS��+H+
D.2HS��+Cu2+��CuS��+H2S��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��W��ԭ������������������ֶ�����Ԫ�أ�A��B��C��D��F�������е����ֻ�����Ԫ����ɵĻ����E����ZԪ���γɵĵ��ʣ�0.1molL-1 D��Һ��pHΪ13��25����������������ͼת����ϵ��������˵����ȷ����
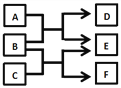
A. ��X��Y��Z��W����Ԫ����ɵ�����ҺpHС��7
B. ������F�к��й��ۼ������Ӽ�
C. 0.1molB������C��ȫ��Ӧ��ת�Ƶ�����Ϊ0.2NA
D. ZԪ�ص��������Ϊ��6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A. ij�л���ȼ��ֻ����CO2��H2O���Ҷ������ʵ�����ȣ�����л�������ΪCnH2n
B. ��ͬ����������ȫȼ�գ�����O2Խ�࣬���к�H��Խ��
C. һ������������������ȼ�ղ�ͨ��ŨH2SO4�����ٵ�������������ɵ�ˮ���������
D. ij��̬��CxHy������������ǡ����ȫ��Ӧ�������Ӧǰ������������䣨�¶ȣ�100������y=4���������С����y��4������y��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������̬����ɵĻ��������ȫȼ�գ��õ�CO2��H2O��������������������ʵ��õĹ�ϵ��ͼ��ʾ��
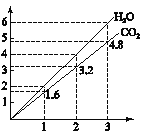
��һ����C2H4�� ��һ����CH4����һ����C3H8 ��һ��û��C2H6�� �ݿ�����C2H2��������C3H4
�������Ըû�������ж���ȷ����
A. �ڢۢ� B. �ݢ� C. �ڢܢ� D. �٢�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com