
| A、KOH溶液 |
| B、Al(OH)3胶体 |
| C、盐酸 |
| D、NaNO3溶液 |


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
| A、HClO4中氯元素化合价比HClO中氯元素化合价高,所以,HClO4的氧化性强 |
| B、具有强氧化性和强还原性的物质放在一起就能发生氧化还原反应 |
| C、已知还原性:B->C->D-,反应2C-+D2=2D-+C2和反应 2C-+B2=2B-+C2都能发生 |
| D、已知①Fe+Cu2+=Fe2++Cu;②2Fe3++Cu=2Fe2++Cu2+,则氧化性强弱顺序为:Fe3+>Cu2+>Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、7.8g由Na2S和Na2O2组成的混合物中含有阴离子的数目为0.1NA |
| B、0.1mol苯中含有双键的数目为0.3NA |
| C、标准状况下,22.4L乙醇中含有分子的数目为NA |
| D、在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化钡溶液与盐酸的反应 2OH-+2H+=2H2O |
| B、钠和冷水反应 Na+2H2O=Na++2OH-+H2↑ |
| C、铜片插入硝酸银溶液中 Cu+Ag+=Cu2++Ag |
| D、碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
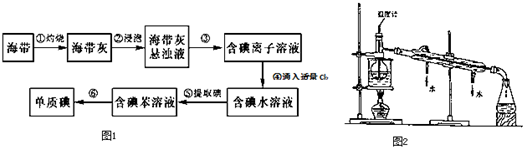
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学式 | AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
| 溶度积 | 1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 5.0×10-13 | 8.3×10-17 |
| A、五种物质在常温下溶解度最大的是Ag2SO4 |
| B、向AgCl的悬浊液中加入0.1mol/L Na2S溶液,则可以生成黑色的Ag2S沉淀 |
| C、外界条件改变时,沉淀溶解平衡也会发生移动 |
| D、常温下,向AgI的悬浊液中加入0.1mol/L NaCl溶液,黄色沉淀变成白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com