
| A、碳酸钠溶于水中 CO32-+2H2O?H2CO3+2OH- |
| B、氯化亚铁溶液中通入少量氯气 Fe2++Cl2=Fe3++2Cl- |
| C、NH4HCO3溶液与过量NaOH稀溶液反应 NH4++OH-=NH3?H2O |
| D、少量Ba(OH)2溶液与NaHSO4溶液反应 Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |


科目:高中化学 来源: 题型:
| A、三种元素所形成的氧化物均为酸性氧化物 |
| B、三者的单质直接与氧气反应都能至少生成两种氧化物 |
| C、CO2、NO2、SO2都能与H2O反应,其反应原理相同 |
| D、相同温度下,等物质的量浓度的Na2CO3、NaNO3、Na2SO3溶液的pH大小顺序:NaNO3<Na2SO3<Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.1 mol/L |
| B、4.2 mol/L |
| C、0.7 mol/L |
| D、1.6 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C4H8O的羧酸与C4H10O的醇反应生成的酯最多有8种 |
| B、葡萄糖与果糖、淀粉与纤维素均互为同分异构体 |
| C、C3H8的二氯代物共有3种 |
| D、C8H10属于芳香烃的同分异构体为3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、磁性氧化铁溶于稀硝酸:3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O |
| B、Na2S2O3溶液中加入稀盐酸:2S2O32-+2H+=SO42-+3S↓+H2O |
| C、100ml0.1mol/L FeI2溶液与标况下0.224L Cl2:2Fe2++Cl2=2Fe3++2Cl- |
| D、向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH-=2 Al(OH)3↓+3BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
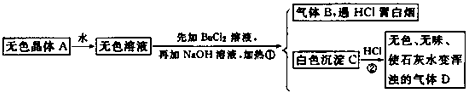
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molFe分别放入足量的冷的浓HNO3、稀HNO3中,反应后转移的电子数均为3NA |
| B、室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA |
| C、标准状况下,22.4LH2O的分子数约为NA个 |
| D、电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少64g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、江河入海口处形成三角洲 |
| B、不同血型的人不能相互输血 |
| C、在FeCl3溶液中滴加NaOH溶液出现红褐色沉淀 |
| D、清晨的阳光穿过茂密林木枝叶所产生的美丽景象(美丽的光线) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com