
分析 (1)由离子交换关系,氢氧根离子物质的量等于氯离子物质的量等于氢离子物质的量,据此计算0.54g FeClx中氯离子物质的量计算x值;
(2)根据元素守恒计算氯化亚铁和氯化铁物质的量之比,进而计算氯化铁质量分数;氯化亚铁用铁和稀盐酸反应生成,氯化铁可以直接用铁和氯气反应得到.
解答 解:(1)n(Cl-)=n(H+)=n(OH-)=0.0250L×0.40 mol•L-1=0.010 mol,则$\frac{0.54g}{(56+35.5x)g/mol}$=0.010 mol,解得x=3,
故答案为:3;
(2)设混合物中FeCl2物质的量为x,FeCl3的物质的量为y,则(x+y):(2x+3y)=1:2.1,得到x:y=9:1,氯化铁物质的量分数=$\frac{1}{1+9}$×100%=10%;
在实验室中,FeCl2可用铁粉和盐酸反应得到,FeCl3可用铁粉和氯气反应生成,
故答案为:10%;盐酸;氯气.
点评 本题考查滴定计算、混合物计算等,是对学生综合能力的考查,需要学生具备扎实的基础,(1)注意利用电荷守恒解答,难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用pH试纸测定溶液的pH时,若先用蒸馏水润湿试纸一定会导致测定结果偏大 | |
| B. | 蒸馏时,应使温度计水银球放在蒸馏烧瓶的支管口处 | |
| C. | 盛放NaOH溶液时,可以使用带玻璃瓶塞的磨口瓶 | |
| D. | .用广泛pH试纸测得0.10 mol•L-1 NH4Cl溶液的pH为5.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡晶体和氯化铵晶体的反应 | |
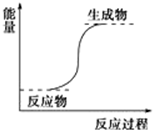
| B. | 能量变化如图所示的反应 | |
| C. | 化学键断裂吸收的能量比化学键形成放出的能量少的反应 | |
| D. | 不需要加热就能发生的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
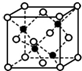 前四周期A、B、C、D、E、F、G原子序数依次增大,A元素的质子数和质量数相等,B元素具有三个能级且所排电子数相同,D元素2p能级上电子数是2s能级的两倍;D和E相邻且同主族.F是第四周期未成对电子最多的原子,G是目前使用量最多的金属.
前四周期A、B、C、D、E、F、G原子序数依次增大,A元素的质子数和质量数相等,B元素具有三个能级且所排电子数相同,D元素2p能级上电子数是2s能级的两倍;D和E相邻且同主族.F是第四周期未成对电子最多的原子,G是目前使用量最多的金属.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ZY、ZW 的水溶液都显酸性 | |
| B. | 原子半径大小:W>R>X,离子半径大小:Z+>R2->W->Y- | |
| C. | W 的氢化物水溶液的酸性比 R 的氢化物水溶液的酸性强,可证明非金属性:W>R | |
| D. | Z、X 两种元素可形成的 Z2X、Z2X2等多种离子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com