
ΓΨΧβΡΩΓΩ¥ΦΥα ς÷§ «“Μ÷÷≥…ΡΛ–‘ΚΟΒΡ ς÷§Θ§œ¬Οφ «“Μ÷÷¥ΦΥα ς÷§ΒΡΚœ≥…œΏ¬ΖΘΚ
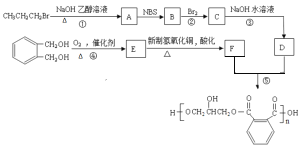
“―÷ΣΘΚRCH2CH=CH2![]()
![]()
Θ®1Θ©”–ΜζΈοA÷–Κ§”–ΒΡΙΌΡήΆ≈ «____________Θ®ΧνΚΚΉ÷Θ©ΘΜ–¥≥ωBΒΡΫαΙΙΦρ Ϋ «______________ΘΜEΒΡΖ÷Ή” ΫΈΣ_____________________ΓΘ
Θ®2Θ©ΔΌΒΡΜ·―ßΖΫ≥Χ Ϋ «____________________________________Θ§ τ”Ύ_______Ζ¥”ΠΓΘ
Θ®3Θ©Ζ¥”ΠΔΌ-Δή÷– τ”Ύ»Γ¥ζΖ¥”ΠΒΡ «________Θ®Χν–ρΚ≈Θ©ΓΘ
Θ®4Θ©Ζ¥”ΠΔήΒΡΜ·―ßΖΫ≥Χ ΫΈΣ «________________________________________ΓΘ
Θ®5Θ©–¥≥ωΖϊΚœœ¬Ν–ΧθΦΰΒΡ”κ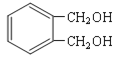 ΜΞΈΣΆ§Ζ÷“λΙΙΧεΒΡΫαΙΙΦρ Ϋ ______________ΓΘ
ΜΞΈΣΆ§Ζ÷“λΙΙΧεΒΡΫαΙΙΦρ Ϋ ______________ΓΘ
aΘ°Φ”»κ¬»Μ·Χζ»ή“ΚΚσœ‘Ήœ…Ϊ
bΘ°Ά®ΙΐΚΥ¥≈Ι≤’ώΖΔœ÷Θ§±ΫΜΖ…œ÷Μ”–ΝΫ÷÷≤ΜΆ§Μ·―ßΜΖΨ≥ΒΡ«βΘ§«“ΖεΟφΜΐ±»ΈΣ1ΘΚ1
cΘ°ΡήΖΔ…ζœϊ»ΞΖ¥”Π
ΓΨ¥πΑΗΓΩΧΦΧΦΥΪΦϋ CH2=CHCH2Br C8H6O2 CH3CH2CH2Br+NaOH ![]() CH3CH=CH2
CH3CH=CH2 ![]() +NaBr+H2O œϊ»ΞΖ¥”Π Δέ
+NaBr+H2O œϊ»ΞΖ¥”Π Δέ  +O2
+O2![]()
 +2 H2O
+2 H2O 
ΓΨΫβΈωΓΩ
ΗυΨίΝς≥ΧΩ…÷ΣΘ§CH3CH2CH2Br‘ΎNaOHΒΡ¥Φ»ή“ΚΦ”»»ΒΡΧθΦΰœ¬ΖΔ…ζœϊ»ΞΖ¥”ΠΘ§…ζ≥…AΘ§ΈΣCH3CH=CH2ΘΜΗυΨί“―÷ΣΘ§A”κNBSΖΔ…ζΖ¥”Π‘Ύ”κΧΦΧΦΥΪΦϋœύΝΎΧΦ‘≠Ή”…œ“ΐ»κ“ΜΗωδε‘≠Ή”Θ§‘ρBΒΡΫαΙΙΦρ ΫΈΣCH2=CHCH2BrΘΜB”κδεΖΔ…ζΦ”≥…Ζ¥”ΠΘ§…ζ≥…CΘ§ΫαΙΙΦρ ΫΈΣCH2BrCHBrCH2BrΘΜC‘Ύ«β―θΜ·ΡΤΥ°»ή“Κ÷–Υ°Ϋβ…ζ≥…±ϊ»ΐ¥ΦΘ§Φ¥DΘΜ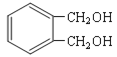 ¥ΏΜ·―θΜ·…ζ≥…ΝΎ±ΫΕΰΦΉ»©Θ§‘Ό”κ–¬÷ΤΒΡ«β―θΜ·Ά≠Ζ¥”Π…ζ≥…ΝΎ±ΫΕΰΦΉΥαΘ§Φ¥FΓΘ
¥ΏΜ·―θΜ·…ζ≥…ΝΎ±ΫΕΰΦΉ»©Θ§‘Ό”κ–¬÷ΤΒΡ«β―θΜ·Ά≠Ζ¥”Π…ζ≥…ΝΎ±ΫΕΰΦΉΥαΘ§Φ¥FΓΘ
Θ®1Θ©Ζ÷ΈωΩ…÷ΣΘ§”–ΜζΈοAΒΡΫαΙΙΦρ ΫΈΣCH3CH=CH2Θ§Κ§”–ΒΡΙΌΡήΆ≈ΈΣΧΦΧΦΥΪΦϋΘΜBΒΡΫαΙΙΦρ ΫΈΣCH2=CHCH2BrΘΜEΒΡΫαΙΙΦρ ΫΈΣ![]() Θ§‘ρΖ÷Ή” ΫΈΣC8H6O2ΘΜ
Θ§‘ρΖ÷Ή” ΫΈΣC8H6O2ΘΜ
Θ®2Θ©ΔΌΈΣCH3CH2CH2Br‘ΎNaOHΒΡ¥Φ»ή“ΚΦ”»»ΒΡΧθΦΰœ¬ΖΔ…ζœϊ»ΞΖ¥”ΠΘ§ΖΫ≥Χ ΫΈΣCH3CH2CH2Br+NaOH ![]() CH3CH=CH2
CH3CH=CH2 ![]() +NaBr+H2OΘΜ
+NaBr+H2OΘΜ
Θ®3Θ©Ζ¥”ΠΔΌΈΣœϊ»ΞΖ¥”ΠΘΜΖ¥”ΠΔΎΈΣΦ”≥…Ζ¥”ΠΘΜΖ¥”ΠΔέΈΣ»Γ¥ζΖ¥”ΠΘΜΖ¥”ΠΔήΈΣ―θΜ·Ζ¥”ΠΘ§¥πΑΗΈΣΔέΘΜ
Θ®4Θ©Ζ¥”ΠΔήΈΣ¥Φτ«ΜυΒΡ¥ΏΜ·―θΜ·Θ§ΖΫ≥Χ ΫΈΣ![]() + O2
+ O2![]()
![]() +2H2OΘΜ
+2H2OΘΜ
Θ®5Θ©![]() ΒΡΖ÷Ή” ΫΈΣC8H10O2Θ§aΘ°Φ”»κ¬»Μ·Χζ»ή“ΚΚσœ‘Ήœ…ΪΘ§Ω…≈–ΕœΚ§”–±ΫΜΖΓΔτ«ΜυΘ§«“τ«Μυ”κ±ΫΜΖ÷±Ϋ”œύΝ§ΘΜbΘ°Ά®ΙΐΚΥ¥≈Ι≤’ώΖΔœ÷Θ§±ΫΜΖ…œ÷Μ”–ΝΫ÷÷≤ΜΆ§Μ·―ßΜΖΨ≥ΒΡ«βΘ§«“ΖεΟφΜΐ±»ΈΣ1ΘΚ1Θ§±ΫΜΖ…œ”–2Ηω»Γ¥ζΜυΘ§«“ΈΣΕ‘≥ΤΫαΙΙΘΜcΘ°ΡήΖΔ…ζœϊ»ΞΖ¥”ΠΘ§Νμ“ΜΗω―θ‘≠Ή”ΈΣτ«ΜυΘ§ΤδΫαΙΙΦρ ΫΈΣ
ΒΡΖ÷Ή” ΫΈΣC8H10O2Θ§aΘ°Φ”»κ¬»Μ·Χζ»ή“ΚΚσœ‘Ήœ…ΪΘ§Ω…≈–ΕœΚ§”–±ΫΜΖΓΔτ«ΜυΘ§«“τ«Μυ”κ±ΫΜΖ÷±Ϋ”œύΝ§ΘΜbΘ°Ά®ΙΐΚΥ¥≈Ι≤’ώΖΔœ÷Θ§±ΫΜΖ…œ÷Μ”–ΝΫ÷÷≤ΜΆ§Μ·―ßΜΖΨ≥ΒΡ«βΘ§«“ΖεΟφΜΐ±»ΈΣ1ΘΚ1Θ§±ΫΜΖ…œ”–2Ηω»Γ¥ζΜυΘ§«“ΈΣΕ‘≥ΤΫαΙΙΘΜcΘ°ΡήΖΔ…ζœϊ»ΞΖ¥”ΠΘ§Νμ“ΜΗω―θ‘≠Ή”ΈΣτ«ΜυΘ§ΤδΫαΙΙΦρ ΫΈΣ![]() Μρ
Μρ ΓΘ
ΓΘ


 Οϊ–ΘΩΈΧΟœΒΝ–¥πΑΗ
Οϊ–ΘΩΈΧΟœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–Ρή”Οά’…≥ΧΊΝ–‘≠άμΫβ ΆΒΡ «
A. FeΘ®SCNΘ©3»ή“Κ÷–Φ”»κΙΧΧεKSCNΚσ―’…Ϊ±δ…ν
B. ΉΊΚλ…ΪBr2’τΤχΦ”―ΙΚσ―’…Ϊ±δ…ν
C. SO2¥ΏΜ·―θΜ·≥…SO3ΒΡΖ¥”ΠΘ§ΆυΆυ–η“Σ Ι”Ο¥ΏΜ·ΦΝ
D. H2ΓΔI2ΓΔHIΤΫΚβΜλΚΆΤχΦ”―ΙΚσ―’…Ϊ±δ…ν
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΆΦ Ψ”κΕ‘”Π–π ωœύΖϊΒΡ «
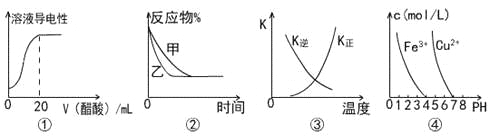
A.ΆΦΔΌ±μ Ψœρ20 mL 0.1 mol/LΑ±Υ°÷–÷πΒΈΦ”»κ0.1 mol/L¥ΉΥαΘ§»ή“ΚΒΦΒγ–‘ΥφΦ”»κΥαΧεΜΐΒΡ±δΜ·
B.ΆΦΔΎ±μ Ψ―Ι«ΩΕ‘Ω…ΡφΖ¥”ΠA(g)+2B(g)![]() 3C(g)+D(s)ΒΡ”ΑœλΘ§““ΒΡ―Ι«Ω±»ΦΉΒΡ―Ι«Ω¥σ
3C(g)+D(s)ΒΡ”ΑœλΘ§““ΒΡ―Ι«Ω±»ΦΉΒΡ―Ι«Ω¥σ
C.ΆΦΔέ÷–«ζœΏ±μ ΨΖ¥”Π3A(g) + B(g)![]() 2CΘ®gΘ©ΓςHΘΦ0Θ§’ΐΓΔΡφΖ¥”ΠΒΡΤΫΚβ≥Θ ΐKΥφΈ¬Ε»ΒΡ±δΜ·
2CΘ®gΘ©ΓςHΘΦ0Θ§’ΐΓΔΡφΖ¥”ΠΒΡΤΫΚβ≥Θ ΐKΥφΈ¬Ε»ΒΡ±δΜ·
D.ΨίΆΦΔήΘ§»τ“Σ≥ΐ»ΞCuSO4»ή“Κ÷–ΒΡFe3+Θ§Ω…Φ”»κNaOH»ή“Κ÷ΝpH‘Ύ4Ήσ”“
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΉνΫϋΘ§ΩΤ―ßΦ“”ΟΒΣΜ·φâ≤ΡΝœ”κΆ≠ΉιΉΑ»γΆΦΥυ ΨΒΡ»ΥΙΛΙβΚœœΒΆ≥Θ§ Βœ÷ΝΥ“‘CO2ΚΆH2OΈΣ‘≠Νœ÷Τ±ΗCH4ΚΆO2œ¬Ν–”–ΙΊΥΒΖ®÷–’ΐ»ΖΒΡ «( )
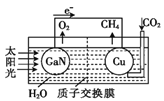
A. ΗΟΉΑ÷Ο÷Μ”–Μ·―ßΡήΉΣΜ·ΈΣΒγΡή
B. ΒΣΜ·οΊΒγΦΪ «“θΦΪ
C. ΒΦœΏ÷–Ψ≠Ιΐ2molΒΡΒγΉ”Θ§ΒΣΜ·οΊΒγΦΪ…ζ≥…lmol O2
D. Ά≠ΒγΦΪ±μΟφΒΡΒγΦΪΖ¥”Π ΫΘΚCO2+8e-+8H+=CH4+2H2O
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥Ά§―ß…ηΦΤ»γΆΦΥυ ΨΉΑ÷Ο÷Τ±Η“ΜœθΜυΦΉ±ΫΓΘ
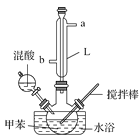
Β―ι≤Ϋ÷η»γœ¬ΘΚ
ΔΌ≈δ÷Τ≈®ΝρΥαΚΆ≈®œθΥα(Α¥ΧεΜΐ±»1ΓΟ3)ΒΡΜλΚœΈο(ΜλΥα)ΘΜ
ΔΎ‘Ύ»ΐΨ±ΤΩάοΉΑ15 mLΦΉ±ΫΘΜ
ΔέΉΑΚΟΤδΥϊ“©ΤΖΘ§≤ΔΉιΉΑΚΟ“«ΤςΘΜ
Δήœρ»ΐΨ±ΤΩ÷–Φ”»κΜλΥαΘ§≤Δ≤ΜΕœΫΝΑηΘΜ
ΔίΩΊ÷ΤΈ¬Ε»Θ§¥σ‘ΦΖ¥”Π10Ζ÷÷”÷Ν»ΐΨ±ΤΩΒΉ”–¥σΝΩ“ΚΧε(Β≠ΜΤ…Ϊ”ΆΉ¥)≥ωœ÷ΘΜ
ΔόΖ÷άκ≥ω“ΜœθΜυΦΉ±ΫΓΘ(“―÷ΣΘΚΦΉ±ΫΒΡΟήΕ»ΈΣ0.866 gΓΛcmΘ≠3Θ§Ζ–ΒψΈΣ110.6 ΓφΘΜœθΜυ±ΫΒΡΟήΕ»ΈΣ1.20 gΓΛcmΘ≠3Θ§Ζ–ΒψΈΣ210.9 Γφ)
ΗυΨί…œ ω Β―ιΘ§ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1) Β―ιΖΫΑΗ÷–»±…Ό“ΜΗω±Ί“ΣΒΡ“«ΤςΘ§Υϋ «________ΓΘ±Ψ Β―ιΒΡΙΊΦϋ «ΩΊ÷ΤΈ¬Ε»‘Ύ30 ΓφΉσ”“Θ§»γΙϊΈ¬Ε»ΙΐΗΏΘ§≤ζ…ζΒΡΚσΙϊ «__________________________ΓΘ
(2)Φρ ω≈δ÷ΤΜλΥαΒΡΖΫΖ®ΘΚ________________________________Θ§≈®ΝρΥαΒΡΉς”Ο «_________________ΓΘ
(3)L“«ΤςΟϊ≥Τ «________Θ§ΫχΥ°ΩΎ «________ΓΘ
(4)–¥≥ωΦΉ±Ϋ”κΜλΥαΖ¥”Π…ζ≥…Ε‘œθΜυΦΉ±ΫΒΡΜ·―ßΖΫ≥Χ ΫΘΚ______________Θ§Ζ¥”Πάύ–ΆΈΣΘΚ________ΓΘ
(5)Ζ÷άκ≤ζΤΖΖΫΑΗ»γœ¬ΘΚ

≤ΌΉς1ΒΡΟϊ≥Τ «________ΓΘ
(6)Ψ≠≤βΕ®Θ§≤ζΤΖ1ΒΡΚΥ¥≈Ι≤’ώ«βΤΉ÷–”–3ΗωΖεΘ§‘ρΤδΫαΙΙΦρ ΫΈΣ________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“―÷ΣH2A‘ΎΥ°÷–¥φ‘Ύ“‘œ¬ΤΫΚβΘΚH2A=H++HA-Θ§HA-![]() H++A2-ΓΘ
H++A2-ΓΘ
Θ®1Θ©NaHA»ή“ΚΒΡpH___(Χν¥σ”ΎΓΔ–Γ”ΎΜρΒ»”Ύ)Na2A»ή“ΚΒΡpHΓΘ
Θ®2Θ©Ρ≥Έ¬Ε»œ¬Θ§»τœρ0.1mol/LΒΡNaHA»ή“Κ÷–÷πΒΈΒΈΦ”0.1mol/LKOH»ή“Κ÷Ν»ή“Κ≥ ÷––‘ΓΘ¥Υ ±ΗΟΜλΚœ»ή“Κ÷–œ¬Ν–ΙΊœΒ÷–Θ§“ΜΕ®’ΐ»ΖΒΡ «___ΓΘ
A.c(H+)ΓΛc(OH-)=1ΓΝ10-14 B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+) D.c(Na+)+c(K+)=0.05mol/L
Θ®3Θ©“―÷Σ≥ΘΈ¬œ¬H2AΒΡΗΤ―Έ(CaA)ΒΡ±ΞΚΆ»ή“Κ÷–¥φ‘Ύ“‘œ¬ΤΫΚβΘΚCaA(s)![]() Ca2+(aq)+A2-(aq) ΠΛHΘΨ0ΓΘ»τ“Σ ΙΗΟ»ή“Κ÷–Ca2+≈®Ε»±δ–ΓΘ§Ω…≤…»ΓΒΡ¥κ ©”–___ΓΘ
Ca2+(aq)+A2-(aq) ΠΛHΘΨ0ΓΘ»τ“Σ ΙΗΟ»ή“Κ÷–Ca2+≈®Ε»±δ–ΓΘ§Ω…≤…»ΓΒΡ¥κ ©”–___ΓΘ
A.…ΐΗΏΈ¬Ε» B.ΫΒΒΆΈ¬Ε» C.Φ”»κNH4ClΨßΧε D.Φ”»κNa2AΙΧΧε
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘Ύ≥ΘΈ¬œ¬Θ§”–œ¬Ν–Έε÷÷»ή“ΚΘΚA.0.1mol/LNH4Cl B.0.1mol/L CH3COONH4 C.0.1mol/LNH4HSO4 D.0.1mol/LNH4HCO3 E.0.1mol/LNaHCO3
«κΗυΨί“Σ«σΧν–¥œ¬Ν–Ω’ΑΉΘΚ
Θ®1Θ©»ή“ΚA≥ ___–‘(ΧνΓΑΥαΓ±ΓΔΓΑΦνΓ±ΜρΓΑ÷–Γ±)Θ§Τδ‘≠“ρ «ΘΚ___(”ΟάκΉ”ΖΫ≥Χ Ϋ±μ Ψ)ΓΘ
Θ®2Θ©»ή“ΚE≥ ___–‘(ΧνΓΑΥαΓ±ΓΔΓΑΦνΓ±ΜρΓΑ÷–Γ±)Θ§Τδ‘≠“ρ «ΘΚ___(”ΟάκΉ”ΖΫ≥Χ Ϋ±μ Ψ)ΓΘ
Θ®3Θ©±»Ϋœ»ή“ΚAΓΔC÷–c(NH4+)ΒΡ¥σ–ΓΙΊœΒ «A___C(ΧνΓΑ>Γ±ΓΔΓΑ<Γ±ΜρΓΑ=Γ±)ΓΘ
Θ®4Θ©≥ΘΈ¬œ¬Θ§≤βΒΟ»ή“ΚBΒΡpH=![]() Θ§‘ρCH3COO-ΒΡΥ°Ϋβ≥ΧΕ»___NH4+ΒΡΥ°Ϋβ≥ΧΕ»(ΧνΓΑ>Γ±ΓΔΓΑ<Γ±ΜρΓΑ=Γ±)Θ§CH3COO-”κNH4+≈®Ε»ΒΡ¥σ–ΓΙΊœΒ «ΘΚc(CH3COO-)___c(NH4+)(ΧνΓΑ>Γ±ΓΔΓΑ<Γ±ΜρΓΑ=Γ±)ΓΘ
Θ§‘ρCH3COO-ΒΡΥ°Ϋβ≥ΧΕ»___NH4+ΒΡΥ°Ϋβ≥ΧΕ»(ΧνΓΑ>Γ±ΓΔΓΑ<Γ±ΜρΓΑ=Γ±)Θ§CH3COO-”κNH4+≈®Ε»ΒΡ¥σ–ΓΙΊœΒ «ΘΚc(CH3COO-)___c(NH4+)(ΧνΓΑ>Γ±ΓΔΓΑ<Γ±ΜρΓΑ=Γ±)ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΫΪ“ΜΗυΫœ¥ΩΧζΑτ¥Ι÷±ΟΜ»κΥ°÷–Θ§”…”Ύ…νΥ°¥Π»ή―θΝΩΫœ…ΌΘ§“ΜΕΈ ±ΦδΚσΖΔœ÷ABΕΈ≤ζ…ζΫœΕύΧζ–βΘ§BCΕΈΗ· ¥―œ÷ΊΘ§œ¬Ν–ΙΊ”Ύ¥Υœ÷œσΒΡΥΒΖ®¥μΈσΒΡ «
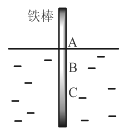
A.ΧζΑτABΕΈΖΔ…ζΖ¥”ΠΈΣO2+ 4e-+ 2H2O = 4OH-
B.Η· ¥Ιΐ≥Χ÷–‘ΎΧζΑτ…œΜα≤ζ…ζΈΔΒγΝςΘ§«“ΖΫœρ «ABΕΈΒΫBCΕΈ
C.œρΥ°÷–Φ”»κ“ΜΕ®ΝΩΝρΥαΦΊΙΧΧεΚσΘ§Ε‘ΧζΑτΒΡ…ζ–βΥΌ¬ ΦΗΚθΈό”Αœλ
D.≤ζ…ζ’β÷÷œ÷œσΒΡ±Ψ÷ ‘≠“ρ «ΧζΑτΥυ¥ΠΒΡΜ·―ßΜΖΨ≥≤ΜΆ§
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–¬±¥ζΧΰ‘ΎKOH¥Φ»ή“Κ÷–Φ”»»≤ΜΖΔ…ζœϊ»ΞΖ¥”ΠΒΡ «Θ® Θ©
ΔΌ![]() ΔΎ
ΔΎ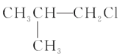 Δέ(CH3)3CCH2Cl ΔήCHCl2-CHBr2 Δί
Δέ(CH3)3CCH2Cl ΔήCHCl2-CHBr2 Δί![]() ΔόCH3Cl
ΔόCH3Cl
A.ΔΌΔέΔόB.ΔΎΔέΔίC.»Ϊ≤ΩD.ΔΎΔή
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com