
| A. | 2种 | B. | 4种 | C. | 9种 | D. | 13种 |
分析 分子式为C5H10O2的有机物A在硫酸作催化剂时得到两种相对分子质量相等的产物,应为酯的水解,可生成羧酸和醇,分别为CH3COOH、CH3CH2CH2OH,以此解答.
解答 解:分子式为C5H10O2的有机物A在硫酸作催化剂时得到两种相对分子质量相等的产物,应为酯的水解,可生成羧酸和醇,分别为CH3COOH、CH3CH2CH2OH,则A的可能结构是CH3COOCH2CH2CH3,CH3COOCH(CH3)2.
故选A.
点评 本题考查有机物的推断,为高频考点,侧重于学生的分析能量和计算能力的考查,本题注意根据相对分子质量关系确定醇和酸的种类,为解答该题的关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:2 | C. | 2:3 | D. | 5:6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可以确定该微粒为Ne | |
| B. | 对应元素的单质可能是强还原剂 | |
| C. | 对应元素可能是电负性最大的元素 | |
| D. | 对应元素可能位于元素周期表中第13列 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 卤族元素 | 氟 | 氯 | 溴 | 碘 |
| 第一电离能(kJ•mol-1) | 1681 | 1251 | 1140 | 1008 |
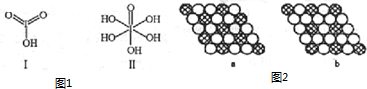
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
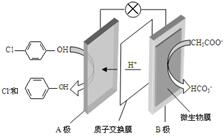 现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚,其原理如图所示,下列说法正确的是( )
现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚,其原理如图所示,下列说法正确的是( )| A. | 电流方向从B极沿导线经小灯泡流向A极 | |
| B. | A极的电极反应式为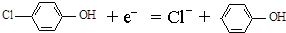 | |
| C. | 当外电路中有0.2mole-转移时,通过质子交换膜的H+的个数为0.2NA | |
| D. | B极为电池的正极,发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
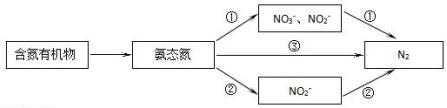
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 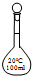 100mL容量瓶 100mL容量瓶 | B. |  100mL集气瓶 | C. | 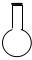 100mL烧瓶 | D. |  100mL滴瓶 100mL滴瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
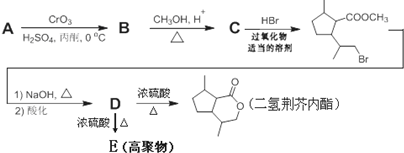
 ,B含有的非氧官能团的名称碳碳双键.C与HBr发生的反应类型是加成反应.
,B含有的非氧官能团的名称碳碳双键.C与HBr发生的反应类型是加成反应.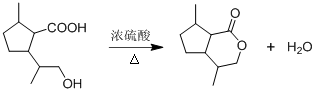 .
. .
. ,其分子中最多有8个碳原子在同一平面上.
,其分子中最多有8个碳原子在同一平面上.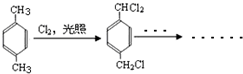
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
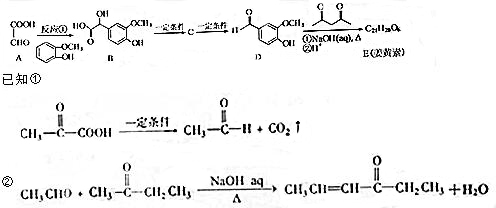
 .
.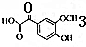 .
.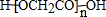 .
. ,下列有关E的叙述正确的是ac.
,下列有关E的叙述正确的是ac.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com