
| A. | 澄清石灰水 | B. | 溴水 | C. | 碳酸钠溶液 | D. | 紫色石蕊试液 |
分析 乙酸、乙醇都易溶于水,但乙酸具有酸性,而苯不溶于水,可用能与乙酸反应、且有明显现象的物质鉴别,以此解答该题.
解答 解:A.乙酸与澄清石灰水发生中和反应,但没有明显现象,乙醇易溶于水,用澄清石灰水不能鉴别乙酸和乙醇,故A错误;
B.加入溴水,乙酸和乙醇都不反应,且混溶,不能鉴别,故B错误;
C.乙酸酸性比碳酸强,与碳酸氢钠溶液反应生成二氧化碳气体,溶液有气泡产生,乙醇与水混溶,苯不溶于水,密度比水小,溶液分层,可鉴别,故C正确;
D.乙酸具有酸性,能使石蕊试液变红色,乙醇为中性液体,不能使石蕊试液变色,苯与水分层,可鉴别,故D正确.
故选CD.
点评 本题考查有机物的鉴别,为高频考点,侧重于学生的分析、实验能力的考查,题目难度不大,本题注意三种物质的性质的差异性,当出现不同现象时才能鉴别.


科目:高中化学 来源: 题型:选择题
| A. | 该元素位于元素周期表的第三周期ⅦA族 | |
| B. | 生成的盐含有的化学键既有离子键又有共价键 | |
| C. | 该元素的常见化合价有:-1、0、+1、+3、+5、+7等 | |
| D. | 该元素的氢化物的稳定性比PH3、H2S弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
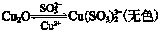
| 操作 | 现象 |
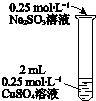 | i 有黄色沉淀出现,随着 Na2SO3溶液的滴入,沉淀增加,当加到5mL时,溶液的蓝色消失. ii 将试管加热,黄色沉淀变为砖红色,有刺激性气味气体产生. iii在加热条件下,继续滴入Na2SO3溶液,砖红色沉淀减少,当1加到10mL时,沉淀完全溶解,得无色溶液. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制取乙炔时,用饱和食盐水代替蒸馏水,以得到平稳的气流 | |
| B. | 除去苯中的少量苯酚:加入适量NaOH溶液,振荡、静置、分液 | |
| C. | 液态溴乙烷中加入稀NaOH溶液共煮几分钟,然后加入足量稀硝酸,再加入AgNO3溶液检验溴乙烷中是否含有溴元素 | |
| D. | 检验甲酸中是否混有乙醛,可向样品中加入足量NaOH溶液以中和甲酸,再做银镜反应或与新制Cu(OH)2共热的实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
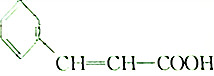
| A. | 该物质能与Na发生反应生成H2 | B. | 该物质能发生加聚反应 | ||
| C. | 该物质在一定件下可发生酯化反应 | D. | 物质的摩尔质量为148 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
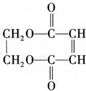 )可用于生产合成树脂、合成橡胶等.以丙烯为原料制备环酯J的合成路线如图
)可用于生产合成树脂、合成橡胶等.以丙烯为原料制备环酯J的合成路线如图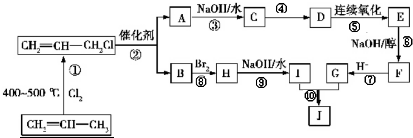
 +3NaOH$→_{△}^{乙醇}$ NaOOC-CH=CH-COONa+NaCl+3H2O;
+3NaOH$→_{△}^{乙醇}$ NaOOC-CH=CH-COONa+NaCl+3H2O;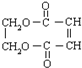 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
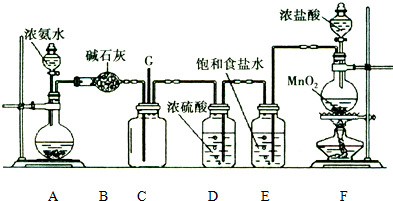
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
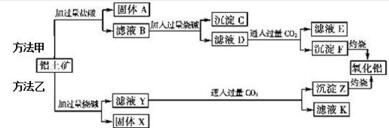
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18g冰晶体中含有氢键的数目为2NA | |
| B. | 1molH2O2中含有非极性键的数目为NA | |
| C. | 1molSiO2晶体中含有Si-O键的数目为4NA | |
| D. | 22.4LHF(标准状况)中含有氟原子的数目为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com