
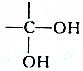 结构的有机物不能稳定存在,根据以上信息,试回答:
结构的有机物不能稳定存在,根据以上信息,试回答: +2H2O,是酯化反应.
+2H2O,是酯化反应. 分析 1molA+1mol NaOH→正盐,说明A中有一个羧基,1mol A$\stackrel{足量Na}{→}$1.5mol气体,说明每个A中有1个羧基外还有两个羟基,A+RCOOH(或ROH)$\stackrel{一定条件}{→}$有香味的物质(R为烃基),说明A中有羧基或羟基,根据信息两个羟基不能连在同一个碳上,以及A的分子式C4H8O4可知,若A分子中含有甲基,A为CH3CH(OH)CH(OH)COOH或CH3C(CH2OH)OHCOOH,A分子中羟基和羧基能脱水生成酯基,据此答题;
解答 解:1molA+1mol NaOH→正盐,说明A中有一个羧基,1mol A$\stackrel{足量Na}{→}$1.5mol气体,说明每个A中有1个羧基外还有两个羟基,A+RCOOH(或ROH)$\stackrel{一定条件}{→}$有香味的物质(R为烃基),说明A中有羧基或羟基,根据信息两个羟基不能连在同一个碳上,以及A的分子式C4H8O4可知,若A分子中含有甲基,A为CH3CH(OH)CH(OH)COOH或CH3C(CH2OH)OHCOOH,A分子中羟基和羧基能脱水生成酯基,
(1)根据上面的分析可知,A的结构中肯定含有的官能团是羟基和羧基,
故答案为:羟基和羧基;
(2)根据上面的分析可知,A的结构简式为CH3CH(OH)CH(OH)COOH或CH3C(CH2OH)OHCOOH,
故答案为:CH3CH(OH)CH(OH)COOH或CH3C(CH2OH)OHCOOH;
(3)A分子内脱水均可形成有香味的四元环状化合物,其反应的化学方程式为2CH3CH(OH)CH(OH)COOH$→_{△}^{浓H_{2}SO_{4}}$ +2H2O,该反应为酯化反应,
+2H2O,该反应为酯化反应,
故答案为:2CH3CH(OH)CH(OH)COOH$→_{△}^{浓H_{2}SO_{4}}$ +2H2O,是酯化反应;
+2H2O,是酯化反应;
点评 本题主要考查了有机物之间的相互转化,难度不大,解题的关键是A物质的确定,答题时注意根据A的分子式和A的性质确定A的结构.


科目:高中化学 来源: 题型:选择题
| A. | Ca2+的结构示意图为: | |
| B. | 氯仿的化学式:CHCl3 | |
| C. | R2+离子核外有a个电子,b个中子,R原子表示为a+ba+b+2R | |
| D. | 溴化氢分子的电子式: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 形成它的小分子结构简式为CH2=CHCOOR(R为烃基) | |
| B. | 在一定条件下能发生加成反应 | |
| C. | 在一定条件下能发生水解反应 | |
| D. | 没有固定的熔沸点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
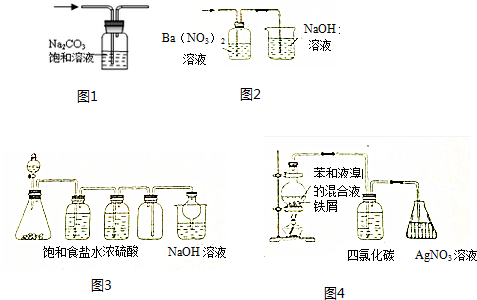
| A. | 用图1装置出去CO2中混有的HCl气体 | |
| B. | 用图2装置除去SO2中混有的SO3气体 | |
| C. | 用图3装置可以制备并收集Cl2 | |
| D. | 用图4装置证明苯与液溴能发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 以石墨作电极电解氯化镁溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| B. | 澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| C. | 氯气通入蒸馏水中 Cl2+H2O═Cl-+ClO-+2 H+ | |
| D. | 次氯酸钠溶液中通入SO2气体:2ClO-+SO2+H2O═2HClO+SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com