
【题目】下列说法错误的是(NA为阿伏加德罗常数的值) ( )
A. 硫酸的摩尔质量是98 g
B. 1molO2的质量是32g/mol
C. 2g氢气所含原子数目为2NA
D. 标准状况下,11.2LCH4的物质的量为0.5mol
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案科目:高中化学 来源: 题型:
【题目】有关下列两套装置的描述不正确的是( ) 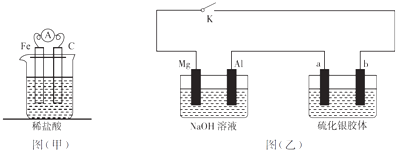
A.甲装置为铁的析氢腐蚀,若将铁换成铜,则甲装置就是铜的吸氧腐蚀
B.若将甲装置中的电流表改为电源,无论电源怎么连接,C电极上都会有气体放出
C.乙装置中K关闭后,a极附近颜色逐渐加深变黑
D.若将乙装置中的NaOH溶液换为HCl溶液,则K关闭后b极颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟在自然界中常以CaF2的形式存在.
(1)下列关于CaF2的表述正确的是 .
a.Ca2+与F﹣间仅存在静电吸引作用
b.F﹣的离子半径小于Cl﹣ , 则CaF2的熔点高于CaCl2
c.阴阳离子比为2:1的物质,均与CaF2晶体构型相同
d.CaF2中的化学键为离子键,因此CaF2在熔融状态下能导电
(2)CaF2难溶于水,但可溶于含Al3+的溶液中,原因是(用离子方程式表示).
已知AlF63﹣在溶液中可稳定存在.
(3)F2通入稀NaOH溶液中可生成OF2 , OF2分子构型为 , 其中氧原子的杂化方式为
(4)F2与其他卤素单质反应可以形成卤素互化物,例如ClF3、BrF3等.已知反应Cl2(g)+3F2(g)═2ClF3(g)△H=﹣313kJmol﹣1 , F﹣F键的键能为159kJmol﹣1 , Cl﹣Cl键的键能为242kJmol﹣1 , 则ClF3中Cl﹣F键的平均键能为kJmol﹣1 . ClF3的熔、沸点比BrF3的(填“高”或“低”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅蓄电池的工作原理为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,研读图,下列判断不正确的是( ) 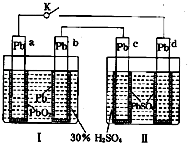
A.K闭合时,d电极反应式:PbSO4+2H2O﹣2e﹣=PbO2+4H++SO42﹣
B.当电路中转移0.2mol电子时,I中消耗的H2SO4为0.2 mol
C.K闭合时,II中SO42﹣向c电极迁移
D.K闭合一段时间后,II可单独作为原电池,d电极为正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中的B~K分别代表有关反应的一种反应物或生成物,其中A、C、F、K是固体;E是常见的气体单质.固态物质A加热后生成的气体混合物若通过碱石灰只剩余气体B,若通过浓硫酸则只剩余气体D.各物质间的转化关系如图所示: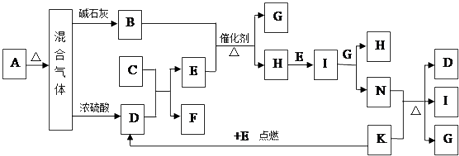
请回答下列问题:
(1)写出实验室检验A物质中含有的阳离子的方法
(2)B与E反应得到1molH,则此时转移电子的物质的量为mol.
(3)写出实验室制取B的化学方程式 .
(4)写出N的稀溶液与过量的铁粉反应的离子方程式 .
(5)若混合气体通过碱石灰得到的气体B与通过浓硫酸得到的气体D的物质的量之比是8:5,则用物质的量的关系表示此固体A的组成为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是部分短周期元素原子半径与原子序数的关系图。则下列说法正确的是
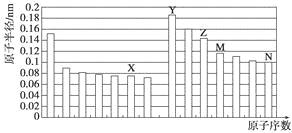
A. Z、N两种元素的离子半径相比,前者较大
B. X、N两种元素的气态氢化物的沸点相比,前者较低
C. 由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应
D. Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列仪器:①烧杯;②锥形瓶;③圆底烧瓶;④试管;⑤坩埚;其中可以用酒精灯直接加热的仪器是( )
A. ①②③④ B. ④⑤ C. ①③ D. ④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人类生产、生活中处处都有化学的身影,下列说法正确的是( )
A.燃放焰火必然会发生化学反应,故焰色反应属于某些金属元素的化学性质
B.水蒸气的液化、煤的液化都属于物质状态的改变,都属于物理变化
C.玻璃属于混合物、水玻璃属于纯净物
D.利用厨房中的食醋和纯碱可证明醋酸酸性强于碳酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com