
����Ŀ���������Ϊ10mL�����ʵ���Ũ����ͬ������NaOH��Һ�зֱ�ͨ��һ������CO2�õ���Һ���ҡ���ס�������Һ�зֱ�μ�0��1 mol��L-1���ᣬ��ʱ��Ӧ����CO2�������״�������������������Ĺ�ϵ��ͼ��ʾ����������������ȷ����
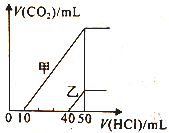
A. ԭNaOH��Һ�����ʵ���Ũ��Ϊ0.5 mol��L-1
B. ��0<V(HCl)<10mLʱ������Һ�з�����Ӧ�����ӷ���ʽΪOH-+H+=H2O
C. ����Һ�к��е�������Na2CO3��NaHCO3
D. ����Һ�еμ���������CO2��������ֵΪ224mL����״����
���𰸡�A
��������������������Һ��ͨ��һ�����Ķ�����̼����Һ�����ʵ���ɿ�����NaOH��Na2CO3��Na2CO3��Na2CO3��NaHCO3��NaHCO3���������û�в���������̼ʱ�ķ�Ӧ����Ϊ��OH-+H+=H2O��CO32-+H+=HCO3-������������̼�ķ�ӦΪ��HCO3-+H+=H2O+CO2����A������ͼ���֪����V(HCl)=50mLʱ���õ��IJ���ΪNaCl����ԭ���غ��֪��n(NaOH)=n(NaCl)=n(HCl)=0.1mol/L��0.05L=0.005mol����ԭ����������Һ��Ũ��Ϊ��c(NaOH)= ![]() =0.5mol/L����A��ȷ��B��������������Һ��ͨ��һ�����Ķ�����̼����Һ�����ʵ���ɿ����ǣ�NaOH��Na2CO3��Na2CO3��Na2CO3��NaHCO3��NaHCO3�����������ͼ��HCl �����������������̼��������Ĺ�ϵ��֪����Һ������Ӧ��Ϊ��Na2CO3��NaHCO3�����Ե�0��V(HCl)��10mLʱ������Һ��û�в���������̼�����ӷ���ʽΪ��CO32-+H+=HCO3-����B����C������������Һ��ͨ�������̼�����ʲ�����ΪNaOH��NaHCO3������ͼ���֪������Һ�е�����ΪNaOH��Na2CO3����C����D������Һ�еμ����ᣬ����������̼�Ľ�Ϊ��HCO3-+H+=H2O+CO2��������������10mL�����֪�����ɶ�����̼�����ʵ���Ϊ��0.1mol/L��0.01L=0.001mol�������0.001mol������̼�����ʵ���Ϊ��22.4L/mol��0.001mol=22.4mL����D����ѡA��
=0.5mol/L����A��ȷ��B��������������Һ��ͨ��һ�����Ķ�����̼����Һ�����ʵ���ɿ����ǣ�NaOH��Na2CO3��Na2CO3��Na2CO3��NaHCO3��NaHCO3�����������ͼ��HCl �����������������̼��������Ĺ�ϵ��֪����Һ������Ӧ��Ϊ��Na2CO3��NaHCO3�����Ե�0��V(HCl)��10mLʱ������Һ��û�в���������̼�����ӷ���ʽΪ��CO32-+H+=HCO3-����B����C������������Һ��ͨ�������̼�����ʲ�����ΪNaOH��NaHCO3������ͼ���֪������Һ�е�����ΪNaOH��Na2CO3����C����D������Һ�еμ����ᣬ����������̼�Ľ�Ϊ��HCO3-+H+=H2O+CO2��������������10mL�����֪�����ɶ�����̼�����ʵ���Ϊ��0.1mol/L��0.01L=0.001mol�������0.001mol������̼�����ʵ���Ϊ��22.4L/mol��0.001mol=22.4mL����D����ѡA��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ҫ����ա�
��1�����и���������ԭ���������ɴ�С��˳������Ϊ������ţ�__________________��
��0.5molCO2 �ڱ�״���£�22.4L���� ��4��ʱ��18mLˮ ��0.2molH2SO4
��2������������Ϊ28%��KOHˮ��Һ�У�OH-��H2O�ĸ���֮��Ϊ__________��
��3������H2SO4��HNO3��CH3COOH��NaOH��Ba(OH)2��Cu(OH)2��ˮ��Һ�н��з�Ӧ���������ӷ���ʽH++OH��=H2O�ķ�Ӧ��__________����
��4����ҵ�������������������ռ���Һ�п����Ʊ���ˮ���������ƣ��Բ���������ѧ��Ӧ����ʽ����ƽFe(NO3)3+Cl2+NaOH����________________________________________��
��5����mg�����뺬��H2SO4��CuSO4��Һ��ȫ��Ӧ������ȫ���ܽ⣬���õ�mgͭ����μӷ�Ӧ��H2SO4��CuSO4�����ʵ���֮��Ϊ_____________��
��6��һ�������£��������ʿ���ͨ�����Ϸ�Ӧ�Ƶõ��У�д��ţ�______________________��
��С�մ� �������� ���Ȼ����� �ܴ��������� ��ͭ�̣���ʽ̼��ͭ�� ����������
��7������þ���Ͻ�10.2g����������500mL4mol/L�������г�ַ�Ӧ������ʣ�࣬����Ӧ�����Һ�м���1000mL�ռ���Һ��ʹ�ó����ﵽ���ֵ���������ռ�����ʵ���Ũ��Ϊ____mol/L��
��8��ij�����ĵ����������һ����̼�ڴ����������³�ַ�Ӧ�����ɵ����Ͷ�����̼����������ɵĵ����Ͷ�����̼�����ʵ���֮��Ϊ1:2����õ���������Ļ�ѧʽΪ_____________��
��9��п���ϡ�����ᷴӦ��������п������狀�ˮ��������amol����пʱ������ԭ����������ʵ���Ϊ______________________mol��
��10����һ������п��100mL18.5mol/LŨ�����ַ�Ӧ��п��ȫ�ܽ⣬ͬʱ����16.8��������壬����Ӧ�����Һϡ�͵�1L�������Һ��c(H+)=1mol/L����������SO2Ϊ________________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ߴ������������ȶ�������������ζ����ʳƷ��ҩƷ����ױƷ������ɫ���� ijʵ��С���ù�ҵFeCl3��Ʒ(��Ca��Mn��Cu����������)Ϊԭ�ϣ�����ȡ��Y(���춡����ͪ)��ȡ����ȡ�ߴ���������ʵ������е���Ҫ�����������£�
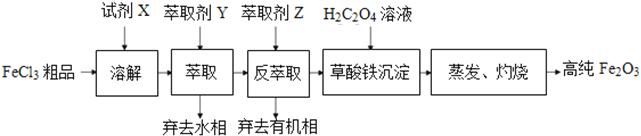
��֪���Լ�X��Ũ���ᣬHCl(Ũ)+FeCl3![]() HFeCl4
HFeCl4
��ش��������⣺
��1��������ʵ����������жϣ�����ʵ��װ���У�û���õ�����_________(�����)
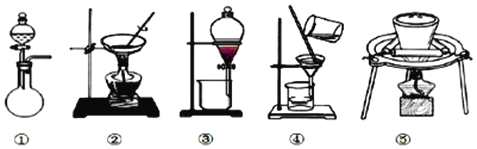
��2������ȡ��Y��ȡ�IJ����У�
��Ca��Mn��Cu���������Ӽ�������_________ (�ˮ�����л���)���С�
�ڷ�Һʱ��Ϊ��֤Һ��˳�����£�Ӧ��_________���ٴ����������²�Һ����ȫ����ʱ���ر��������ٴ��Ͽڵ����ϲ�Һ�塣
��3���Ʊ���ȡ��Y(���춡����ͪ)ʱ����ֲ�Ʒ�к���������ͪ��4-��-2-�촼���������ʵ����ʡ�һ��ɲ����������ᴿ������ʱ��Ӧ���¶ȼ�ˮ��������_________������ǰ��Ԥ�����ֲ�Ʒʱ����������_________ϴ(����ѡ�Լ���Ӧ����ĸ����ͬ)������_________ϴ�������_________ϴ��
Aˮ B̼��������Һ C�Ҵ�
��4�������Լ��У�����ȡ��Z�����ѡ����_________������ȡ�ܷ�����ԭ����_________(�ӻ�ѧƽ��ĽǶȽ��н���)��
A���ߴ�ˮ B������ C��ϡ���� D���ƾ�
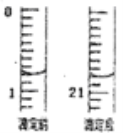
��5���ⶨ��Ʒ���������ĺ����辭���ܡ���ԭΪFe2+��Ȼ���������������ñ� K2Cr2O7��Һ�ζ�(��ԭ������Cr3+�����ʲ���K2Cr2O7��Ӧ)����ȷ��ȡ1.0g��Ʒ�����ܡ���ԭΪFe2+����0.1000mol/L�ı���Һ���еζ���
�ٵζ���ʼ���յ��Һ��λ����ͼ��������K2Cr2O7����Һ���Ϊ_________mL��
�ڲ�Ʒ���������ĺ���Ϊ_________(������λ��Ч����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1 ���������2 ��������ǡ����ȫ��������2 �������壨ͬ��ͬѹ������������ķ���ʽΪYX2������ҵķ���ʽ����Ϊ
A��X2 ��Y2 B��XY ��X2 C�� X2 ��YX D��YX ��Y2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϡ�ļ�����Һ����ˮ���ݣ���ʹ�������߲��ϵ�ũҩ���Ͷ��ԣ����ü�����Һ�����߲ˣ�����ˮ�м��������ģ�������
A.��
B.����
C.����
D.ʳ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ʵ��С����Ƶ�����ʵ������������ ��������
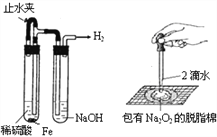
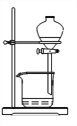
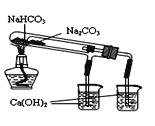
A. ͼ1���Ʊ����۲����������� B. ͼ2��֤������������ˮ��Ӧ����
C. ͼ3����ȡ��Һʱ�ų���ı���Һ D. ͼ4���Ƚ�NaHCO3��Na2CO3���ȶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ÿ��10��23������6:02������6:02����Ϊ��Ħ����"(Mole Day),���ʱ�����ʽд��Ϊ6:0210/23������밢���ӵ�����6.02��1023���ơ�NAΪ�����ӵ�������ֵ������˵����ȷ����
A. ��״����22.4 LNO��11.2LO2 ��ַ�Ӧ������ķ�����ΪNA
B. 0.1mol/L��Na2SO4��Һ����SO42- ��Ŀ��0.1NA
C. ��״����.22.4L�������������۳�ַ�Ӧ,ת�Ƶĵ�����Ϊ3NA
D. 0.1molCH4�ĺ��������ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ù����һ����Ч�������أ�������ˮ���õ���ù�ذ�������ӵĽṹ��ʽ��ͼ�����й��ڸ����ʵ���������ȷ���ǣ� �� 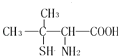
A.���ڦ���������
B.�ܷ����Ӿ۷�Ӧ���ɶ���
C.�˴Ź��������Ϲ���5����
D.��ù�ع��������ᵼ����������ҩǰһ��Ҫ����Ƥ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���ס��ҡ���Ϊ�������ʣ��׳�����Ϊ���壬��Ϊһ����ɫ���壬��Ϊ��ɫ���塣A��B��C��D��Ϊ�����DΪһ���ɫ����������֮������ͼת����ϵ��
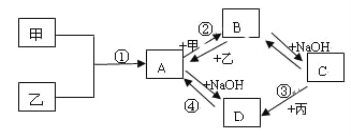
��ش��������⡣
��1��д���������ʵ����ƣ���____________��B______________��
��2��д���۷�Ӧ�Ļ�ѧ����ʽ��_____________________________��
��3��д���ڷ�Ӧ�����ӷ���ʽ��____________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com