
 已知:2NaOH+Cl2=NaClO+NaCl+H2O.标准状况下,H2和 Cl2的混合气体共2.24L,光照充分反应后,用NaOH充分吸收.
已知:2NaOH+Cl2=NaClO+NaCl+H2O.标准状况下,H2和 Cl2的混合气体共2.24L,光照充分反应后,用NaOH充分吸收.分析 (1)消耗氢氧钠的量为最大值时,氯气应取最大值2.24L,依据化学方程式定量关系计算得到氢氧化钠的最大值;
(2)氢气和氯气的混合气体2.24L两者反应生成氯化氢,1mol氢气生成2mol氯化氢消耗2mol氢氧化钠,且生成的氯化钠物质的量和1mol氯气和氢氧化钠反应出的氯化钠相同,所以在氢气体积分数小于50%时,氯化钠物质的量始终为0.1mol,当氢气的体积分数多于氯气,由于多于的氢气与氢氧化钠不反应会降低氢氧化钠的消耗量,所以当氢气体积分数大于50%时为曲线的拐点,依次计算得到氢气体积分数为0、25%、50%、75%、100%时的氯化钠物质的量即可得到曲线;
解答 解:(1)消耗氢氧钠的量为最大值时,氯气应取最大值2.24L,标准状况下物质的量=$\frac{2.24L}{22.4L/mol}$=0.1mol,依据化学方程式定量关系计算,2NaOH+Cl2=NaClO+NaCl+H2O得到氢氧化钠的最大值为0.2mol,
故答案为:0~0.2;
(2)氢气和氯气的混合气体2.24L两者反应生成氯化氢,1mol氢气生成2mol氯化氢消耗2mol氢氧化钠,且生成的氯化钠物质的量和1mol氯气和氢氧化钠反应出的氯化钠相同,所以在氢气体积分数小于50%时,氯化钠物质的量始终为0.1mol,当氢气的体积分数多于氯气,由于多于的氢气与氢氧化钠不反应会降低氢氧化钠的消耗量,所以当氢气体积分数大于50%时为曲线的拐点,依次计算得到氢气体积分数为0、25%、50%、75%、100%时的氯化钠物质的量为0.10mol、0.10mol,0.10mol、0.05mol,0即可得到曲线;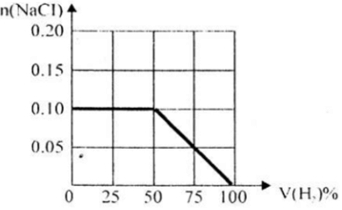 ,
,
故答案为: ;
;
点评 本题考查了物质性质、化学反应定量关系、图象绘制等知识点,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| 酸 | 电离常数(25℃) |
| 碳酸 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
| 次溴酸 | Ka=2.4×10-9 |
| A. | HBrO+Na2CO3═NaBrO+NaHCO3 | B. | 2HBrO+Na2CO3═2NaBrO+H2O+CO2↑ | ||
| C. | HBrO+NaHCO3═NaBrO+H2O+CO2↑ | D. | NaBrO+NaHCO3═Na2CO3+HBrO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沉淀物 | Fe(OH)3 | Mn(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 2.7 | 8.3 | 4.2 |
| 完全沉淀的pH | 3.2 | 9.8 | 6.7 |
| 序号 | 1 | 2 | 3 |
| 起始读数 | 0.95mL | 0.70mL | 1.00mL |
| 终点读数 | 20.95mL | 24.95mL | 21.00mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食用白糖的主要成分是蔗糖 | B. | 纤维素不能水解成葡萄糖 | ||
| C. | 蛋白质水解的最终产物是多肽 | D. | 植物油的主要成分是高级脂肪酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2与水反应:3NO2+H2O═2NO3-+NO+2H+ | |
| B. | 向亚硫酸钠溶液中加入足量硝酸:SO32-+2H+═SO2↑+H2O | |
| C. | 氨水吸收NO、NO2:NO+NO2+2OH-═2NO2-+H2O | |
| D. | NH4HCO3溶于过量浓NaOH溶液中:NH4++OH-═NH3↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com