
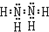 ,燃烧反应为N2H4+O2
,燃烧反应为N2H4+O2
| ||
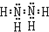 ;N2H4+O2
;N2H4+O2
| ||
 ,
, .
.


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源: 题型:
| A、体积相同,但不一定是22.4L |
| B、分子数相同,但原子数不同 |
| C、摩尔质量不同,但质量相同 |
| D、质子数不同,电子数也不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 相关信息 |
| U | 所处的周期数、族序数分别与其原子序数相等. |
| V | 基态时,电子分布在三个能级上,且各能级中电子数相等. |
| W | 基态时,2P轨道处于半充满状态 |
| X | 与W元素处于同一周期,且X第一电离能小于W的第一电离能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、D、E五种元素其核电荷数依次增大.A原子只有1个s电子,B原子L层中s电子和p电子数目相同,B、C、D属于同周期且相邻,E原子内层均饱和,N层上只有两个电子.
A、B、C、D、E五种元素其核电荷数依次增大.A原子只有1个s电子,B原子L层中s电子和p电子数目相同,B、C、D属于同周期且相邻,E原子内层均饱和,N层上只有两个电子.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、MnO4-、Na+、Cl- |
| B、K+、Na+、NO3-、CO32- |
| C、Na+、H+、NO3-、SO42- |
| D、Mg2+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol?L-1的Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) |
| B、NaA溶液的pH=8,c(Na+)-c(A-)=9.9×10-7 mol?L-1 |
| C、将0.1mol/L的Na2S溶液与0.1mol/L的NaHS溶液等体积混合,所得溶液中:c(OH-)=c(H+)+c(S2-)+2c(HS-)+3c(H2S) |
| D、将25mL0.2mol/L的盐酸与100mL0.1mol/L的氨水混合,所得溶液中:c(Cl-)>c(NH4+)>c(NH3?H2O)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
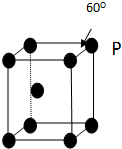
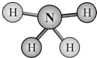 肼(H2N-NH2)和偏二甲肼[H2N-N(CH3)2]均可用作火箭燃料.查阅资料得知,肼是一种良好的极性溶剂,沿肼分子球棍模型的氮、氮键方向观察,看到的平面图如图所示.下列说法不正确的是( )
肼(H2N-NH2)和偏二甲肼[H2N-N(CH3)2]均可用作火箭燃料.查阅资料得知,肼是一种良好的极性溶剂,沿肼分子球棍模型的氮、氮键方向观察,看到的平面图如图所示.下列说法不正确的是( )| A、肼分子中的氮原子采用sp3杂化 |
| B、肼分子中既有极性键又有非极性键 |
| C、肼分子是非极性分子 |
| D、肼与偏二甲肼互称同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com