
下列化学方程式书写正确,且能用离子方程式Ba2++CO32-=BaCO3↓表示的是( )A.Ba(OH)2+CO2=BaCO3↓+H2O
B.Ba(HCO3)+Ba(OH)2=2BaCO3↓+2H2O
C.Ba(NO3)2+Na2CO3=BaCO3↓+2NaNO3
D.Ba(OH)2+2KHCO3=BaCO3↓+KOH+H2O
科目:高中化学 来源:2016-2017学年江西省宜春市高一上月考二化学卷(解析版) 题型:选择题
下列说法中正确的是( )
A.有单质生成的反应一定存在元素化合价的变化
B.化学反应中某元素化合价升高必定存在另一元素化合价降低
C.氧化还原反应的实质是有离子定向移动
D.氧化还原反应不一定都是置换反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省饶阳县高一上期中化学试卷(解析版) 题型:选择题
下列变化中需加入氧化剂才能实现的是( )。
A. Cl-→Cl2 B.Fe3+→Fe2+ C.CuO→Cu D H2SO4→BaSO4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高一上期中化学卷(解析版) 题型:填空题
根据反应①~④四个反应,回答下列问题:
①H2S+I2=S+2HI
②2FeCl2+Cl2=2FeCl3
③Cu+2H2SO4(浓)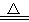 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
④Cl2+2KI=2KCl+I2
(1)反应①的反应类型为(填序号) 。
A.置换反应 B.复分解反应
C.化合反应 D.氧化还原反应
(2)对于反应②,还原剂与氧化剂的物质的量之比为________。
(3)对于反应③,用双线桥法标明电子转移的方向和数目________________________,
(4)写出反应④的离子方程式____ _____________________。
_____________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高一上期中化学卷(解析版) 题型:选择题
下列反应属于氧化还原反应,但水既不作氧化剂又不作还原剂的是( )
A.H2O+CaO = Ca(OH)2 
B.2H2O+2Na = 2NaOH+H2↑
C.3NO2+H2O = 2HNO3+NO
D.2H2O O2↑+2H2↑
O2↑+2H2↑
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高一上期中化学卷(解析版) 题型:选择题
下列电离方程式错误的是 ( )
A.NaHCO3 = Na++H++CO32- B.NaHSO4 = Na++H++SO42-
C.Mg(NO3)2 = Mg2++2NO3- D.Na2SO4 = 2Na++SO42-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高二上期中化学卷(解析版) 题型:选择题
3molA和2.5molB混合于容积为2L的容器内,使它们发生反应2A(s)+3B(g) 2C(g)+D(g),经过5min生成0.5molD,下列说法正确的是( )
2C(g)+D(g),经过5min生成0.5molD,下列说法正确的是( )
A.B的平均消耗速率为0.3mol/(L min)
min)
B.若反应容器内气体的密度不再发生变化,说明反应已经达到平衡
C.平衡后,增大压强,平衡将向正反应方向移动
D.C的平衡浓度为2mol/L
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长株潭岳益五市十校高三12月联考化学卷(解析版) 题型:填空题
(1)汽车剧烈碰撞时,安全气囊中发生反应NaN3+KNO3→K2O+Na2O+X↑(未配平),已知X为单质,在反应中NaN3失去电子.则该反应的氧化剂为______,X的化学式为______.
(2)工业上制取高纯度MnO2的某一步骤如图所示:
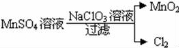
请写出该反应的离子方程式__ ___.
(3)草酸钙晶体(CaC2O4•H2O)可用作分离稀有金属的载体.
①在一定温度下向2L的密闭容器放入足量草酸钙(固体所占体积忽略不计)发生反应:CaC2O4(s)?CaO(s)+CO(g)+CO2(g),若前5min内生成CaO的质量为11.2g,则该段时间内v(CO)=__________mol•L﹣1•min﹣1;当反应达到平衡后,将容器体积压缩到原来的一半,则下列说法正确的是__________(填答案选项编号).
A.平衡不移动,CaO的质量不变
B.平衡发生移动,且CaC2O4的分解率增大
C.平衡发生移动,但CO和CO2的浓度都没有改变
D.平衡向逆反应方向移动,且该反应的化学平衡常数减小
②某温度下,向0.3mol/L的Na2CO3溶液中加入足量CaC2O4粉末后(忽略溶液体积变化),充分搅拌,发生反应:CO32﹣(aq)+CaC2O4(s)?CaCO3(s)+C2O42﹣(aq).静置后沉淀转化达到平衡.求此时溶液中的c(C2O42﹣)= mol•L﹣1.已知:该温度下,KSP(CaC2O4)=5.0×10﹣9;KSP(CaCO3)=2.5×10﹣9.
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省分校高一上期中化学卷(解析版) 题型:实验题
实验室用固体烧碱配制450mL0.25mol·L-1的CuSO4溶液。
(1)需称量_____________g的CuSO4·5H2O固体。
(2)配制过程中,不需要使用的仪器是(填代号)_____________。
①烧杯②量筒③玻璃棒④1000mL容量瓶⑤漏斗⑥500mL试剂瓶
(3)根据实验的实际需要和(2)中列出的仪器判断,完成实验还缺少的玻璃仪器是__________________ (填仪器名称)。
(4)下列操作使配制出的溶液浓度偏低的是(填编号)____________。
A.称量药品时物码放反 |
B.把溶液转移到容量瓶时有溶液溅出 |
C.转移溶液前容量瓶中有蒸馏水 |
D.定容时仰视读数 |
E.定容时俯视读数
F.定容后发现容量瓶中液体超过标线,用胶头滴管吸出一部分
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com