
【题目】乌洛托品在合成、医药、染料等工业中有广泛用途,其结构式如图所示.将甲醛水溶液与氨水混合蒸发可制得乌洛托品.若原料完全反应生成乌洛托品,则甲醛与氨的物质的量之比为( ) 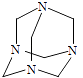
A.1:1
B.2:3
C.3:2
D.2:1
【答案】C
【解析】解:将甲醛水溶液与氨水混合蒸发可制得乌洛托品,若原料完全反应生成乌洛托品,每个乌洛托品分子中含有6个C原子、4个N原子,每个甲醛分子中含有1个C原子、每个氨气分子中含有1个N原子,根据C原子、N原子守恒知,要形成一个乌洛托品分子需要6个甲醛分子、4个氨气分子,则需要甲醛和氨气分子个数之比=6:4=3:2,根据N=nNA知,分子数之比等于物质的量之比,所以甲醛与氨的物质的量之比3:2, 故选C.
将甲醛水溶液与氨水混合蒸发可制得乌洛托品,若原料完全反应生成乌洛托品,每个乌洛托品分子中含有6个C原子、4个N原子,根据C原子、N原子守恒判断甲醛和氨的物质的量之比.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:
【题目】我国发行的第五套人民币中,1元、5角、1角硬币的材料分别为钢芯镀镍合金(1元)、钢芯镀铜合金(5角)和铝合金(1角)。下列说法正确的是( )
A.铸造硬币的合金实际价值低于面值
B.铸造硬币的合金在海水中也不会被腐蚀
C.三种面值不同的硬币材质不同是因为它们的实际价值不同
D.应鼓励人们尽量多地收集硬币
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl36H2O)的工艺流程如图: 
回答下列问题:
(1)煅烧时粉碎硫铁矿的目的是 . 该反应的化学方程式 , 该反应中被氧化的元素是 .
(2)酸溶及后续过程中均需保持盐酸过量,其目的是、;
(3)操作a为蒸发浓缩、冷却结晶、、、干燥,获得FeCl36H2O;
(4)焙烧产生的二氧化硫可以用来生产硫酸,其中利用催化氧化反应将SO2转化为SO3是一个关键步骤.压强及温度对SO2转化率的影响如下表:
0.1 | 0.5 | 1 | 10 | |
400 | 99.2% | 99.6% | 99.7% | 99.9% |
500 | 93.5% | 96.9% | 97.8% | 99.3% |
600 | 73.7% | 85.8% | 89.5% | 96.4% |
根据表中的数据判断该反应的正向属于(填“放热“或”吸热“)反应,理由是 .
(5)计算每生产1万吨98%硫酸所需要含80%FeS2的硫铁矿为吨(假设反应过程中硫的损失率为5%,结果保留一位小数).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中的实验装置可用于制取乙炔.请填空: 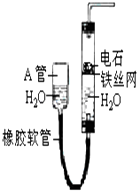
(1)图中,A管的作用是制取乙炔的化学方程式是:
(2)乙炔通入KMnO4酸性溶液中观察到的现象是 , 乙炔发生了反应.
(3)乙炔通入溴的CCl4溶液中观察到的现象是 , 乙炔发生了反应.
(4)为了安全,点燃乙炔前应 , 乙炔燃烧时的实验现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组以废铁屑、稀硫酸、饱和(NH4)2SO4溶液为原料,经过一系列反应和操作后,合成了浅蓝绿色晶体X.为确定其组成,进行如下实验.
I.结晶水的测定:称取7.84g浅蓝绿晶体,加热至100℃失去结晶水,冷却至室温
后,称重,质量为5.68g.
Ⅱ.NH4+的测定:将上述5.68g固体置于如图所示的三颈瓶中,然后逐滴加入足量10% NaOH溶液,通入氮气,用40.00mL l molL﹣1的硫酸溶液吸收产生氨气.蒸氨结束后取下接收瓶,用2molL﹣1NaOH标准溶液滴定过剩的硫酸,到终点时消耗20.00mLNaOH溶液.
Ⅲ.铁元素的测定:将上述实验结束后三颈瓶中的溶液全部倒入锥形瓶中,向其中加入适量3%H2O2的溶液,充分振荡后滤出沉淀,洗净、干燥、灼烧后;测得其质量为1.6g. 回答下列问题:
(1)在实验I中,不可能用到的实验仪器是(填正确答案标号).
A.烧杯
B.铁架台(带铁圈)
C.坩埚
D.蒸发皿
E.酒精灯
F.干燥器
G.托盘天平
(2)在实验Ⅱ中,通入氮气的目的是 . 蒸氨结束后,为了减少实验误差,还需要对直形冷凝管进行“处理”,“处理”的操作方法是
(3)在实验Ⅱ中,用NaOH标准溶液滴定过剩的硫酸时,应使用式滴定管;可使用的指示剂为 .
(4)在实验中,检验沉淀是否洗净的方法是 .
(5)根据上述实验数据计算,该浅蓝绿晶体的化学式为 . 三颈瓶中发生反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F是一种新型涂料固化剂,可由下列路线合成(部分反应条件略去).请回答下列问题: 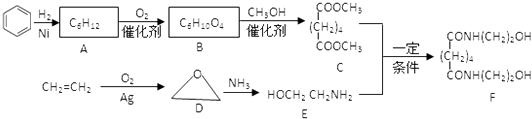
(1)B的结构简式是;E中含有的官能团名称是 .
(2)由C和E合成F的化学方程式是 .
(3)同时满足下列条件的苯的同分异构体的结构简式是 . ①含有3个双键;②核磁共振氢谱只显示1个吸收峰;③不存在甲基
(4)乙烯在实验室可由(填有机物名称)通过(填反应类型)制备,制乙烯时还产生少量SO2、CO2及水蒸气,用以下试剂检验这四种气体,混合气体通过试剂的顺序是 . (填序号). ①过量饱和Na2SO3溶液②酸性KMnO4溶液③石灰水④无水CuSO4⑤品红溶液
(5)下列说法正确的是(填序号). a.A属于饱和烃 b.D与乙醛的分子式相同
c.E不能与盐酸反应 d.F可以发生酯化反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1molN2和3mol H2充入体积可变的恒温密闭容器中,在380℃下发生反应:N2(g)+3H2(g) ![]() 2NH3(g),平衡时,体系中氨的体积分数(NH3)随压强变化的情况如表:
2NH3(g),平衡时,体系中氨的体积分数(NH3)随压强变化的情况如表:
压强/MPa | 10 | 20 | 30 | 40 |
φ(NH3) | 0.30 | 0.45 | 0.54 | 0.60 |
下列说法正确的是( )
A.10 MPa时,H2的转化率为75%
B.20 MPa时,NH3的物质的量浓度是10 MPa时的1.5倍
C.40 MPa时,若容器的体积为VL,则平衡常数 ![]()
D.30 MPa时,若向容器中充入惰性气体,则平衡向正反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com