
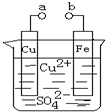
| A. | a和b不连接时,铁片上会有金属铜析出 | |
| B. | a和b用导线连接时,铁片上发生的反应为:Cu2++2e-═Cu | |
| C. | a和b用导线连接时,电子由a流向b | |
| D. | 无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
分析 铁比铜活泼,可置换铜,形成原电池反应时,铁为负极,发生氧化反应,电极方程式为Fe-2e-=Fe2+,铜为正极,发生还原反应,电极方程式为Cu2++2e-=Cu,以此解答.
解答 解:A.a和b不连接时,铁和铜离子发生置换反应而发生化学腐蚀,故A正确;
B.a和b用导线连接时,铁片上发生的反应为Fe-2e-=Fe2+,故B错误;
C.Fe比铜活泼,形成原电池反应时Fe为负极,则电子由b流向a,故C错误;
D.无论a和b是否连接,铁片均会溶解,都生成亚铁离子,溶液由蓝色变为浅绿色,故D正确.
故选AD.
点评 本题考查原电池知识,为高频考点,侧重于学生分析能力和基本理论的理解和运用的考查,注意把握金属的活泼性强弱以及电极方程式的书写,难度不大.


科目:高中化学 来源: 题型:解答题
| 化学键 | C-H | C-F | H-F | F-F | H-H | H-N |
| 键 能 | 414 | 489 | 565 | 158 | 436 | 391 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
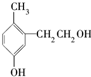
| A. | 它是苯酚的同系物 | |
| B. | 1mol该有机物能与2 mol溴水发生取代反应 | |
| C. | 1mol该有机物能与金属钠反应产生0.5 mol H2 | |
| D. | 1mol该有机物能与2 mol NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 598 | B. | 576 | C. | 288 | D. | 299 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2-丁醇发生消去反应产物有2 种 | B. | 卤代烃都能发生水解反应 | ||
| C. | 醇在Cu/△条件下都能氧化成醛 | D. | 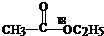 在酸性条件下水解产物是 在酸性条件下水解产物是 和C2H5OH 和C2H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度只提高逆反应速率 | B. | 降低温度正、逆反应速率都降低 | ||
| C. | 催化剂只会增大反应速率 | D. | 减小压强时只是逆反应速率降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将食物保存在电冰箱里 | |
| B. | 做粉尘爆炸实验时选用很细的面粉 | |
| C. | 向过氧化氢溶液中加入MnO2 | |
| D. | 铁与稀盐酸反应太慢时加入较浓的盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子晶体中可能含有共价键,但不一定含有金属元素 | |
| B. | 分子晶体中一定含有共价键 | |
| C. | 非极性分子中一定存在非极性键 | |
| D. | 对于组成和结构相似的分子晶体,一定是相对分子质量越大,熔、沸点越高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com