
| A. | 含大量Al3+的溶液中:Na+、K+、SO42-、HCO3- | |
| B. | 在加入铝粉能产生氢气的溶液中:NH4+、Fe2+、SO42-、NO3- | |
| C. | 含大量OH-的溶液中:Na+、NO3-、K+、AlO2- | |
| D. | 含大量Fe3+的溶液中:NH4+、Na+、I-、SCN- |
分析 A.Al3+与HCO3-相互促进水解;
B.加入铝粉能产生氢气的溶液为非氧化性酸或强碱溶液;
C.碱溶液中该组离子之间不反应;
D.离子之间发生氧化还原反应,离子之间结合生成络离子.
解答 解:A.Al3+与HCO3-相互促进水解,不能大量共存,故A错误;
B.加入铝粉能产生氢气的溶液为非氧化性酸或强碱溶液,碱溶液中不能大量存在NH4+、Fe2+,酸溶液中Fe2+、NO3-发生氧化还原反应,故B错误;
C.碱溶液中该组离子之间不反应,可大量共存,故C正确;
D.Fe3+、I-发生氧化还原反应,Fe3+、SCN-结合生成络离子,不能大量共存,故D错误;
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意水解反应、氧化还原反应,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ |
 ;由H和①形成的原子数之比为1:1的物质
;由H和①形成的原子数之比为1:1的物质 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{49}^{115}$In原子核外有49个电子 | |
| B. | ${\;}_{49}^{115}$In原子核内有49个中子 | |
| C. | ${\;}_{49}^{115}$In原子核内质子数和中子数之和等于其质量数,为115 | |
| D. | ${\;}_{49}^{115}$In是In元素的一种核素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
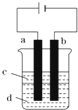 Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.若用如图实验装置可制得纯净的Fe(OH)2沉淀,两极材料分别为石墨和铁.
Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.若用如图实验装置可制得纯净的Fe(OH)2沉淀,两极材料分别为石墨和铁.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所有卤代烃都含有卤原子 | |
| B. | 所有卤代烃都是通过取代反应制得的 | |
| C. | 所有卤代烃在适当条件下都能发生消去反应 | |
| D. | 所有卤代烃都是难溶于水,密度比水小的液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C的反应速率与B的生成速率相等 | |
| B. | 单位时间内生成2n mol A,同时生成3n mol B | |
| C. | A、B、C的浓度不再变化 | |
| D. | A、B、C的浓度之比为1:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 气体 | 除杂试剂 |
| A | CO2(HCl) | 盛饱和NaHCO3溶液的吸气瓶 |
| B | Cl2(HCl) | 盛饱和食盐水的吸气瓶 |
| C | NH3(H2O) | 盛碱石灰的球形干燥管 |
| D | SO2(HCl) | 盛饱和AgNO3溶液的吸气瓶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
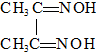 )作用生成腥红色配合物沉淀A.
)作用生成腥红色配合物沉淀A.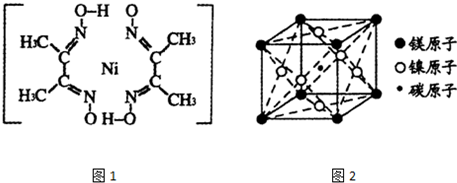
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石膏(CaSO4•2H2O) | B. | 硫铁矿(FeS2) | ||
| C. | 纯碱(NaHCO3) | D. | 芒硝(Na2SO4•10H2O) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com