
【题目】某100 mL溶液可能含有Na+、NH4+、Ca2+、CO32-、SO42-、Cl-中的若干种,取该溶液进行连续实验,实验过程如下(所加试剂均过量,气体全部逸出):
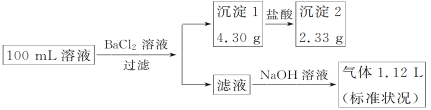
下列说法不正确的是( )
A.原溶液一定存在CO32-和SO42-,一定不存在Ca2+
B.若原溶液中不存在Na+,则c(Cl-)<0.1 mol·L-1
C.原溶液中c(Cl-)≥0.1 mol·L-1
D.原溶液一定存在Cl-,可能存在Na+
【答案】B
【解析】
原溶液中加入BaCl2溶液生成沉淀,原溶液中一定含有CO32-或SO42-中的至少一种,则沉淀1为BaSO4、BaCO3中的至少一种,由沉淀1部分溶解于盐酸可知其一定是BaSO4、BaCO3的混合物,原溶液中一定存在CO32-和SO42-,沉淀2是BaSO4,物质的量为 ![]() ,则BaCO3的物质的量为
,则BaCO3的物质的量为![]() ,CO32-、SO42-与Ca2+均不能共存,原溶液中一定不存在Ca2+。滤液加NaOH溶液生成气体,生成的气体为氨气,则原溶液中一定含有NH4+,由氮元素守恒可知NH4+的物质的量为
,CO32-、SO42-与Ca2+均不能共存,原溶液中一定不存在Ca2+。滤液加NaOH溶液生成气体,生成的气体为氨气,则原溶液中一定含有NH4+,由氮元素守恒可知NH4+的物质的量为![]() ,阳离子所带正电荷的物质的量为0.05mol,CO32-和SO42-所带负电荷的物质的量之和为0.012+0.012=0.04mol,根据电荷守恒可知,原溶液中一定存在有Cl-,Na+不能确定,故n(Cl-)≥0.01mol,原溶液体积为100mL,即c(Cl-)≥0.1 mol·L-1。
,阳离子所带正电荷的物质的量为0.05mol,CO32-和SO42-所带负电荷的物质的量之和为0.012+0.012=0.04mol,根据电荷守恒可知,原溶液中一定存在有Cl-,Na+不能确定,故n(Cl-)≥0.01mol,原溶液体积为100mL,即c(Cl-)≥0.1 mol·L-1。
根据以上分析进行解答。
原溶液中加入BaCl2溶液生成沉淀,原溶液中一定含有CO32-或SO42-中的至少一种,则沉淀1为BaSO4、BaCO3中的至少一种,由沉淀1部分溶解于盐酸可知其一定是BaSO4、BaCO3的混合物,原溶液中一定存在CO32-和SO42-,沉淀2是BaSO4,物质的量为 ![]() ,则BaCO3的物质的量为
,则BaCO3的物质的量为![]() ,CO32-、SO42-与Ca2+均不能共存,原溶液中一定不存在Ca2+。滤液加NaOH溶液生成气体,生成的气体为氨气,则原溶液中一定含有NH4+,由氮元素守恒可知NH4+的物质的量为
,CO32-、SO42-与Ca2+均不能共存,原溶液中一定不存在Ca2+。滤液加NaOH溶液生成气体,生成的气体为氨气,则原溶液中一定含有NH4+,由氮元素守恒可知NH4+的物质的量为![]() ,阳离子所带正电荷的物质的量为0.05mol,CO32-和SO42-所带负电荷的物质的量之和为0.012+0.012=0.04mol,根据电荷守恒可知,原溶液中一定存在有Cl-,Na+不能确定,故n(Cl-)≥0.01mol,原溶液体积为100mL,即c(Cl-)≥0.1 mol·L-1。
,阳离子所带正电荷的物质的量为0.05mol,CO32-和SO42-所带负电荷的物质的量之和为0.012+0.012=0.04mol,根据电荷守恒可知,原溶液中一定存在有Cl-,Na+不能确定,故n(Cl-)≥0.01mol,原溶液体积为100mL,即c(Cl-)≥0.1 mol·L-1。
A.原溶液一定存在CO32-和SO42-,一定不存在Ca2+,A正确;
B.若原溶液中不存在Na+,则c(Cl-)=0.1 mol·L-1,B错误;
C.原溶液中c(Cl-)≥0.1 mol·L-1,C正确;
D.原溶液一定存在Cl-,可能存在Na+,D正确;
答案选B。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】(1)2016年9月G20峰会在杭州举行。
①峰会部分场馆使用了新型环保墙面材料硅藻泥。硅藻泥的主要成分SiO2属于______(填字母,下同)。
a 有机高分子材料 b 无机非金属材料 c 金属材料
②峰会场馆空调使用CO2和水作制冷剂。不用氟利昂作制冷剂的目的是______。
a 防治酸雨 b 降低温室效应 c 保护臭氧层
③央行发行了G20峰会金银合金纪念币。关于该纪念币的说法正确的是______。

a可以溶于盐酸 b 相比纯金币,熔点高c 相比纯金币,硬度大
(2)紫薯营养丰富,具有特殊的保健功能。下表是100 g紫薯粉的营养成分含量表:
营养成分 | 含量(每100 g) | 营养成分 | 含量(每100 g) |
水分 | 9.9 g | 钙元素 | 23.00 mg |
脂肪 | 0.2 g | 铁元素 | 1.10 mg |
蛋白质 | 4.8 g | 硒元素 | 0.02 mg |
淀粉 | 82.5 g | 花青素 | 0.10 g |
纤维素 | 2.7 g | 其他 | …… |
①紫薯粉中的脂肪在人体内会水解成高级脂肪酸和_______。
②紫薯中的花青素能消耗活性氧,具有_______性(选填“氧化”或“还原”),可用于抗衰老。
(3)防治环境污染,呵护生态环境是当今社会的主题之一。
①汽车尾气(含有烃类、CO、NOx、SO2等)是城市空气的主要污染源,治理方法之一是在汽车排气管上加装“催化转化器”使CO、NOx转化为无害物质,下列说法不正确的是_____。
a CO和NOx反应的化学方程式为:2xCO+2NOx 2xCO2+N2
2xCO2+N2
b 上述方法增加了空气中CO2的含量,加重了酸雨污染
c 在日光照射下,汽车尾气还会产生光化学烟雾
②通过水质检测确定水体中污染物的种类和浓度后,可采取不同的方法对污水进行处理。例如向废水中通入臭氧,运用_____(填字母)除去其中含有的油类、氰化物。
A 中和法 b 沉淀法 c 氧化法
③用过的聚乙烯塑料食品袋要回收处理。聚乙烯是由乙烯通过聚合反应得来的,那么乙烯的结构简式是_______。
④锂电池为动力的新能源汽车可实现汽车低碳排放,锂电池属于_______电池(选填“一次”或“二次”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中各微粒的浓度关系正确的是
A.0.1 mol·L-1NaHSO4溶液中:c(Na+)>c(SO42-)>c(H+) >c(OH-)
B.0.1 mol·L-1Na2S溶液中:2 c(Na+)=c(S2-)+c(HS-)+c(H2S)
C.0.1 mol·L-1NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)
D.等体积、等物质的量浓度的乙酸溶液和氢氧化钠溶液混合后:C(Na+)=c(CH3COO-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知水在25℃和95℃时,其电离平衡曲线如图所示:
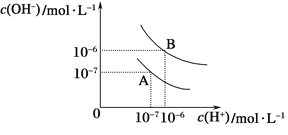
(1)则95℃时水的电离平衡曲线应为__(填“A”或“B”).
(2)25℃时,将pH=9的NaOH溶液与pH=3的H2SO4溶液混合,所得溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为_____
(3)95℃时,若1体积pH1=a 的某强酸溶液与10体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是:___(用含a、b的等式表示).
(4)95℃时,1L0.05mol/LBa(OH)2溶液中,由水电离出的c(OH-)为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,A、B、C、D、E均由上述元素组成的中学化学常见的物质,其中A是单质,C是酸性氧化物,A的水溶液和C均具有漂白性,B是自然界最常见的液体,E是三元化台物,物质之间存在如右下图所示的关系。下列说法不正确的是
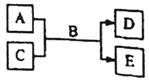
A. YX2遇到蓝色石蕊试液先变红后褪色 B. 离子半径大小关系:Y>Z>X>W
C. 简单阴离子的还原性:Y>Z D. Y与Z属于同一周期,与X属于同一主族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列营养物质在人体内发生的变化及其对人的生命活动所起的作用叙述中,不正确的是( )
A. 淀粉![]() 葡萄糖
葡萄糖![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
B. 纤维素![]() 葡萄糖
葡萄糖![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
C. 油脂![]() 甘油和高级脂肪酸
甘油和高级脂肪酸![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
D. 蛋白质![]() 氨基酸
氨基酸![]() 人体所需的蛋白质(人体生长发育)
人体所需的蛋白质(人体生长发育)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】线型 PAA( ![]() )具有高吸水性,网状 PAA 在抗压性、吸水性等方面优于线型 PAA。网状 PAA 的制备方法是:将丙烯酸用 NaOH 中和,加入少量交联剂 a,再引发聚合。其部分结构片段 如图所示,列说法错误的是
)具有高吸水性,网状 PAA 在抗压性、吸水性等方面优于线型 PAA。网状 PAA 的制备方法是:将丙烯酸用 NaOH 中和,加入少量交联剂 a,再引发聚合。其部分结构片段 如图所示,列说法错误的是
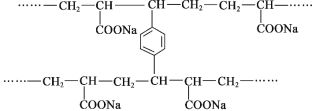
A.线型 PAA 的单体不存在顺反异构现象
B.形成网状结构的过程发生了加聚反应
C.交联剂 a 的结构简式是![]()
D.PAA 的高吸水性与—COONa 有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.100mol/L NaOH 溶液分别滴定20.00mL 0.100mol/L的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是
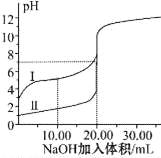
A. Ⅰ、Ⅱ分别表示盐酸和醋酸的滴定曲线
B. V(NaOH)=10.00 mL 时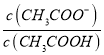 >1
>1
C. pH=7时,两种酸所用NaOH溶液的体积相等
D. V(NaOH)=20.00 mL 时,c(Cl-)<c(CH3COO-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com